| 物竞编号 | 0MU5 |
|---|---|
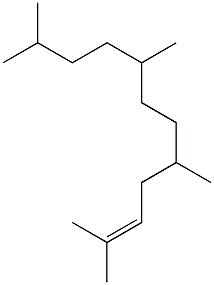
| 分子式 | C16H32 |
| 分子量 | 224.43 |
| 标签 | Isobutene tetramer |
编号系统
CAS号:15220-85-6
MDL号:暂无
EINECS号:暂无
RTECS号:暂无
BRN号:暂无
PubChem号:暂无
物性数据
1. 性状:未确定
2. 密度(g/mL,25/4℃):0.8
3. 相对蒸汽密度(g/mL,空气=1):未确定
4. 熔点(ºC):未确定
5. 沸点(ºC,常压):未确定
6. 沸点(ºC,5.2kPa): 未确定
7. 折射率: 未确定
8. 闪点(ºC): 未确定
9. 比旋光度(º): 未确定
10. 自燃点或引燃温度(ºC): 未确定
11. 蒸气压(kPa,25ºC): 未确定
12. 饱和蒸气压(kPa,60ºC): 未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC): 未确定
15. 临界压力(KPa): 未确定
16. 油水(辛醇/水)分配系数的对数值: 未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V): 未确定
19. 溶解性:未确定
毒理学数据
暂无
生态学数据
暂无
分子结构数据
五、分子性质数据:
1、 摩尔折射率:75.95
2、 摩尔体积(m3/mol):287.1
3、 等张比容(90.2K):644.2
4、 表面张力(dyne/cm):25.3
5、 极化率(10-24cm3):30.10
计算化学数据
1.疏水参数计算参考值(XlogP):7.3
2.氢键供体数量:0
3.氢键受体数量:0
4.可旋转化学键数量:6
5.互变异构体数量:无
6.拓扑分子极性表面积0
7.重原子数量:16
8.表面电荷:0
9.复杂度:201
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
暂无
贮存方法
暂无
合成方法
暂无
用途
暂无
安全信息
危险运输编码:暂无
危险品标志:暂无
安全标识:暂无
危险标识:暂无
文献
暂无
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号