| 物竞编号 | 0K2K |
|---|---|
| 分子式 | K2Cr2O7 |
| 分子量 | 294.19 |
| 标签 | 红矾钾, 二铬酸钾, Potassium dichromate(Ⅵ), 氧化还原滴定剂, 氧化剂, 防腐剂, 媒染剂, 无机缓蚀材料 |
编号系统
CAS号:7778-50-9
MDL号:MFCD00011367
EINECS号:231-906-6
RTECS号:HX7680000
BRN号:暂无
PubChem号:24898340
物性数据
1.性状:橘红色结晶[1]
2.熔点(℃):398[2]
3.沸点(℃):500(分解)[3]
4.相对密度(水=1):2.68[4]
5.溶解性:溶于水,不溶于乙醇,溶于苯、二甲基亚砜。[5]
毒理学数据
1.急性毒性[6] LD50:25mg/kg(大鼠经口);190mg/kg(小鼠经口);14mg/kg(兔经皮)
2.刺激性[7] 家兔经眼:140mg,重度刺激。
3.致突变性[8] 微生物致突变:鼠伤寒沙门菌100μg/皿;大肠杆菌1600μmol/L;酿酒酵母菌60mg/L。微核试验:小鼠腹腔注射50mg/kg。姐妹染色单体交换:小鼠淋巴细胞1μmol/L。
4.致畸性[9] 大、小鼠孕后不同时间经口给予不同剂量,致肌肉骨骼系统、颅面部(包括鼻、舌)、血液和淋巴系统(包括脾和骨髓)发育畸形。
5.致癌性[10] IARC致癌性评论:G1,确认人类致癌物。
6.其他[11] 小鼠经口最低中毒剂量(TDLo):1710mg/kg(孕19d),致胚胎发育迟缓,面部发育异常。
生态学数据
1.生态毒性[12] EC50:1.57mg/L(24h)(水蚤)
2.生物降解性 暂无资料
3.非生物降解性 暂无资料
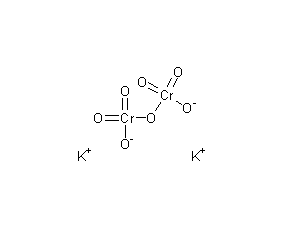
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:7
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积124
7.重原子数量:11
8.表面电荷:0
9.复杂度:194
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:3
性质与稳定性
1.重铬酸钾为强氧化剂,与有机物接触、撞击能引起燃烧。遇强酸或高温时能释出氧气,促使有机物燃烧。与还原剂、有机物、易燃物如硫、磷或金属粉末等混合可形成爆炸性混合物。有水时与硫化钠混合能引起自燃。与硝酸盐、氯酸盐接触剧烈反应。具有较强的腐蚀性。不可与有机物、易燃物、还原剂、强酸等共贮混运。不溶于乙醇,溶于水。常温下在空气中稳定。是强氧化剂。加热至398℃不发生分解而熔融,变成暗褐色的液体,冷却时又恢复原状。加热到500℃分解而放出氧,变成Cr2O3和铬酸钾。
2.稳定性[13] 稳定
3.禁配物[14] 强还原剂、易燃或可燃物、酸类、活性金属粉末、硫、磷
4.避免接触的条件[15] 潮湿空气
5.聚合危害[16] 不聚合
贮存方法
储存注意事项[17] 储存于阴凉、通风的库房。远离火种、热源。库温不宜超过30℃,相对湿度不超过80%。包装密封。应与易(可)燃物、还原剂等分开存放,切忌混储。储区应备有合适的材料收容泄漏物。
合成方法
1.复分解法 将重铬酸钠(或制造重铬酸钠后的母液)稀释加热,加入理论量的氯化钾(含KCl>90%)进行复分解,反应温度为105~110℃,反应溶液浓度控制在37~38°Bé,生成重铬酸钾溶液。加入少量氯酸钠,用氢氧化钠调整溶液Ph值为5~6,再加入少量硫酸铝使杂质絮凝,经澄清除去杂质,将溶液冷却结晶,再经离心分离、洗涤、干燥,制得重铬酸钾成品。其反应方程式如下:
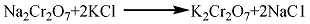
分离后的母液,经浓缩析出氯化钠结晶,而重铬酸钾仍溶于液相。分离氯化钠,并用热洗液和热水洗涤,洗液可与重铬酸钾母液合并进行蒸发。分离氯化钠后的母液经澄清除去不溶物,冷却溶液可再次得到重铬酸钠结晶,二次母液可返回反应器。
2.将硝酸钾、碳酸钾和三氧化二铬均按一定的配比混合,将混合物加热,之后冷却到室温,用热水萃取。将溶液过滤,滤液用浓硫酸化,并将溶液一直加热到结晶出现。冷却后,析出重铬酸钾晶体,随即离心分离。为进一步提纯,结晶物在0~100℃以水为溶剂进行重结晶,然后在150~155℃下真空干燥即可。
3.将工业品重铬酸钾在水溶液中进行再结晶,然后过滤。于110℃下干燥的结晶,在玛瑙研钵中研成细粉,再于120℃下干燥2h。如需要更高纯度,则可先在石英皿中重结晶3次,再用铂皿重结晶3次。将4g铬铁矿粉与4g NaNO3混匀,另取4g NaOH与4g Na2CO3于铁坩埚中混匀。小火加热至熔,然后把矿粉分几次加入并不断搅拌,以防熔物喷溅。矿粉加完后,逐渐加大火焰,灼烧半小时,证其自然冷却。在熔块快要干涸时用力搅拌,倒入烧杯中。附在坩埚内的熔物加少量水,小火加热至沸,取出的熔物转入烧杯中。如此反复2~3次,熔物全部取出后,将烧杯加热煮沸约20min,要不断搅拌使熔块溶解。然后吸滤,滤渣用水洗一次。滤液体积控制在40mL左右。滴加冰醋酸(约4~5mL)调滤液pH为7~8,使Al(OH)3沉淀,加热浓缩到溶液约为原体积2/3时,冷却吸滤,沉淀为Al(OH)3和NaAc·3H2O(回收),滤液转入蒸发皿中。再用冰醋酸(约4mL)调至pH≈5,溶液由黄色转为橙红色。往制得的重铬酸钠溶液加入1.5g KCl,水溶加热,蒸发至表面有晶膜出现,再调pH≈5,水冷却,有大量晶体析出后吸滤。晶体是K2Cr2O7和NaAc·3H2O的混合物,转入蒸发皿滴加沸水至全溶,令其冷却,进行重结晶,吸滤得K2Cr2O7晶体。滤液回收。得到产品在50℃下烘干,称重,计算产率。
用途
1.用于生产铬明矾、氧化铬绿、铬黄颜料。搪瓷工业用它与长石粉、石英砂等混合后煅烧成珐琅粉,作绿色的着色剂。用于调制火柴药头,起氧化防潮作用。用作轻革的鞣革剂。媒介染料染色和印花用作媒染剂。制合成香料用作氧化剂。用于电焊条、印刷油墨,金属钝化。用作有机合成的氧化剂和催化剂及医药品的原料。
2.用作采油酸化压裂液增稠剂、堵水,调剖剂的交联剂,常与聚合物一起配合使用。
3.用作强氧化剂、分析试剂,制烟火,颜料及用于鞣革等方面。
4.由于重铬酸钾具有强氧化性,在表面处理中重铬酸钾曾被大量用于铝及合金的弱碱性化学氧化。这种化学氧化膜层多用于非重要件的防护处理,或用于涂装的底层处理以提高涂层和基体金属的结合力。但弱碱性化学氧化需要在较高的温度下进行,同时六价铬毒性较大,现已较少采用。
5.用于银的浸亮以及锌、银、铅锡合金、铜和铜合金、不锈钢的化学钝化或电解钝化等溶液中。
6.用作缓蚀剂、金属钝化剂、杀菌防腐剂等。还用于电镀、医药等工业。
7.用于皮革、火柴、印染、化学、电镀等工业。[18]
安全信息
危险运输编码:UN 3086 6.1/PG 1
危险品标志: 极毒
极毒  氧化剂
氧化剂  危害环境
危害环境
危险标识:R8 R21 R25 R26 R34 R45 R46 R60 R61 R42/43 R48/23 R50/53 R51/53 R52/53
文献
[1~18]参考书:危险化学品安全技术全书.第一卷/张海峰主编.—2版.北京;化学工业出版社,2007.6 ISBN 978-7-122-00165-8
备注
曾用CAS:7778-52-9




 沪公网安备 31010602001115号
沪公网安备 31010602001115号