| 物竞编号 | 0QUR |
|---|---|
| 分子式 | NaN3 |
| 分子量 | 65.01 |
| 标签 | 防腐剂 |
编号系统
CAS号:26628-22-8
MDL号:MFCD00003536
EINECS号:247-852-1
RTECS号:暂无
BRN号:暂无
PubChem号:暂无
物性数据
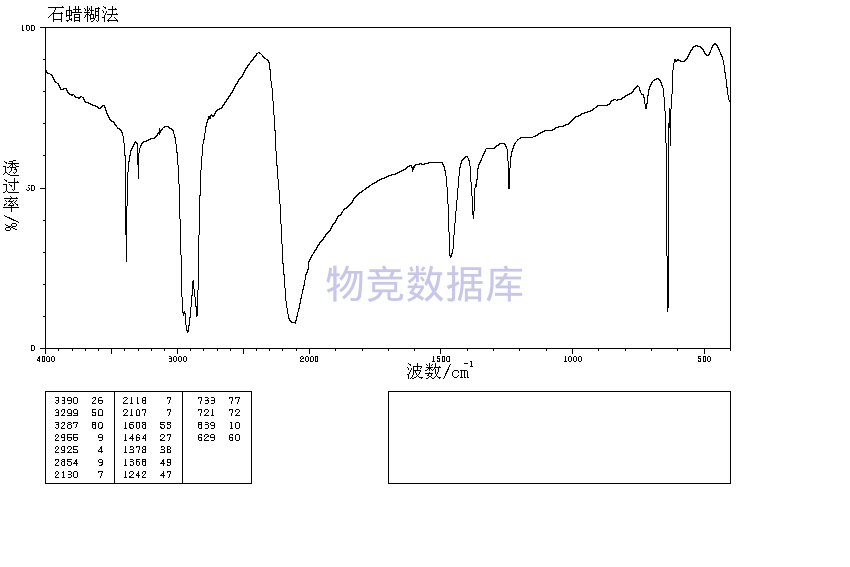
1.性状:无色六角结晶性粉末。[13]
2.熔点(℃):275(分解)[14]
3.相对密度(水=1):1.85[15]
4.相对蒸气密度(空气=1):2.2[16]
5.溶解性:溶于水、液氨,不溶于乙醚,微溶于乙醇。[17]
毒理学数据
1.急性毒性[18]
LD50:27mg/kg(大鼠经口);27mg/kg(小鼠经口);20mg/kg(大鼠经皮);20mg/kg(兔经皮)
2.刺激性 暂无资料
生态学数据
1.生态毒性[19]
LC50:0.8~1.6mg/L(96h)(虹鳟鱼);0.8mg/L(96h)(蓝鳃太阳鱼)
EC50:8.4mg/L(96h)(低额蚤);4.2mg/L(96h)(水蚤)
2.生物降解性 暂无资料
3.非生物降解性 暂无资料
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:2
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积3
7.重原子数量:4
8.表面电荷:0
9.复杂度:15.5
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:2
性质与稳定性
1.在高于其熔点的温度下可分解爆炸;可以与金属、酸和氯化溶剂形成叠氮化物,有爆炸危险;所有用量应很少,操作应该在通风橱中进行;多余的叠氮化钠应该在通风橱中用酸化的亚硝酸钠浸泡或者用四价的硝酸铵铈盐氧化除掉[1]。
叠氮化钠是一种有亲核性的叠氮化物,通常情况下,几何异构的二卤化物与叠氮化钠反应,生成有几何异构的叠氮化物[2];在相同的条件下,也会出现不寻常的腈化物[3]。二氧磷化物的叠氮化开环反应的立体选择与溶剂有很大关系 (式1)[4]。
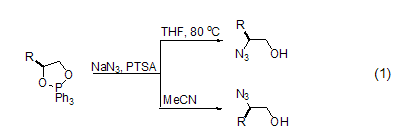
在NH4Cl溶液中,NaN3与环氧酯反应,可以得到产率为60%的产物 (式2)[5]。

在亲核试剂存在下,可以实现异氰酸酯的诱导。一些环酐类物质反应生成异氰酸酯后,可以连续地进行环化。在甲醇中,N-acyloxazo- lidinone与NaN3反应,生成相应的醇 (式3)[6]。此外,酯在NaN3的甲醇溶液中发生裂解,生成醇 (式4) [7]。
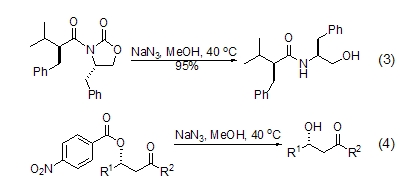
有机叠氮化物与烯烃反应,可以得到三唑啉 (三唑由炔得到)、吖丙啶和其它的杂环化合物[8]。产生的三唑啉随后进行裂解,可以得到其它的杂环化合物 (式5)[9]。叠氮化钠和α,β-不饱和烯烃 (或者炔烃) 反应,根据取代的不同情况得到不同的杂环化合物 (式6)[10]。
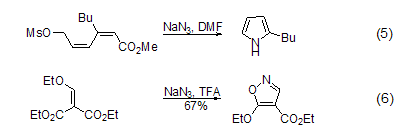
N,N-二乙基甲酰基叠氮化物可以通过NaN3与三乙胺反应制得 (式7)[11]。芳香醛与NaN3在室温下反应,生成芳香醛叠氮化物 (式8)[12]。
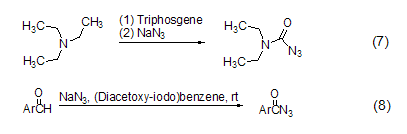
2.稳定性[20] 不稳定
3.禁配物[21] 酸类、酰基氯、活性金属粉末、强氧化剂
4.避免接触的条件[22] 受热、摩擦、震动、撞击
5.聚合危害[23] 不聚合
贮存方法
储存注意事项[24] 储存于阴凉、通风良好的专用库房内,实行“双人收发、双人保管”制度。远离火种、热源。库温不宜超过30℃。包装密封。应与氧化剂、酸类、活性金属粉末、食用化学品分开存放,切忌混储。储区应备有合适的材料收容泄漏物。
合成方法
1.将盛有19.51g(0.5mol)NaNH2的镍盘置于带有密封盖(盖子上开有三个孔,中间安装N2O入口管,两边分别安装出气管和温度计)的铁制容器中。把经过碱石灰和KOH干燥的N2O通到NaNH2上,令其反应5h,得到粗产物,用水重结晶即得到纯品。
2.用制备叠氮化钾的方法,只需要以NaOH取代KOH就可。
3.可用氨基钠与一氧化二氮反应:
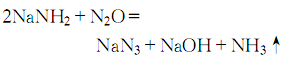
用途
1.用于有机合成、污水含氧量测定、血清防腐剂等。
2.用作分析试剂。用于制备其他叠氮化合物、叠氮酸及纯钠。也可用于细菌培养基的配制。
3.用于制造炸药及用作分析试剂等。[25]
安全信息
危险运输编码:暂无
危险品标志:暂无
安全标识:暂无
危险标识:暂无
文献
1. Bretherick, L.; Handbook of Reactive Chemical Hazards, 4th ed; Butterworths: London, 1990, p 1360. 2. Ogilvie, W.; Rank, W. Can. J. Chem., 1987, 65, 166. 3. Kappe, C. O. Liebigs. Ann. Chem., 1990, 505. 4. Pautard-Copper, A.; Evans, Jr. S. A. Tetrahedron, 1991, 47, 1603. 5. Orr, D. E. Synthesis, 1984, 618. 6. Bouzide, A.; Sauve, G. Tetrahedron Lett., 2002, 43, 1961. 7. Gomez-Vidal, J. A.; Forrester, M. T.; Silverman, R. B. Org.Lett., 2001, 3, 2477. 8. Lwowshi, W. 1,3-Dipolar Cycloaddition Chemistry, Padwa, A. Ed; Wiley: New York, 1984, 773. 9. (a) Sundberg, R. J.; Pearce, B. C. J. Org. Chem., 1982, 47, 725. (b) Choi, J. R.; Han, S.; Cha, J. K. Tetrahedron Lett., 1991, 32, 6469. 10. Donkor, A.; Prager, R. H.; Thompson, M. J. J. Am. Chem. Soc., 1992, 45, 1571. 11. Gumaste, V. K.; Deshmukh, A. R. A. S. Tetrahedron Lett., 2004, 45, 6571. 12. Chen, D. J.; Chen Z. C. Tetrahedron Lett., 2000, 41, 7361. [1~12]参考书:现代有机合成试剂<性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7 [13~25]参考书:危险化学品安全技术全书.第一卷/张海峰主编.—2版.北京;化学工业出版社,2007.6 ISBN 978-7-122-00165-8
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号