| 物竞编号 | 0JWK |
|---|---|
| 分子式 | NaNO2 |
| 分子量 | 69.00 |
| 标签 | 阻聚剂, 发色剂, 媒染剂, 漂白剂, 金属热处理剂, 电镀缓蚀剂, 油墨所用原料及中间体 |
编号系统
CAS号:7632-00-0
MDL号:MFCD00011118
EINECS号:231-555-9
RTECS号:RA1225000
BRN号:暂无
PubChem号:24886427
物性数据
1.性状:白色或淡黄色细结晶,无臭,略有咸味,易潮解。[11]
2.pH值:9(水溶液)[12]
3.熔点(℃):271[13]
4.沸点(℃):320(分解)[14]
5.相对密度(水=1):2.17[15]
6.溶解性:易溶于水,微溶于乙醇、甲醇、乙醚。[16]
毒理学数据
1.急性毒性[17]
LD50:180mg/kg(大鼠经口)
LC50:5.5mg/m3(大鼠吸入,4h)
2.刺激性[18] 家兔经眼:500mg(24h),轻度刺激。
3.致突变性[19] 微生物致突变:鼠伤寒沙门菌属250μg/皿。程序外DNA合成:人Hela细胞6mmol/L。DNA抑制:人成纤维细胞2000ppm。DNA损伤:小鼠淋巴细胞105mmol/L。细胞遗传学分析:猴肝265mg/L。
4.致畸性[20] 大鼠孕后10~19d,腹腔内给予最低中毒剂量(TDLo)400mg/kg,致中枢神经系统发育畸形,血液和淋巴系统发育畸形(包括脾和骨髓)。小鼠多代经口给予最低中毒剂量(TDLo)480mg/kg,致泌尿生殖系统发育畸形。
生态学数据
1.生态毒性 暂无资料
2.生物降解性 暂无资料
3.非生物降解性 暂无资料
4.其他有害作用[21] 该物质对环境有危害,应特别注意对水体的污染。
分子结构数据
1、摩尔折射率:无可用
2、摩尔体积(cm3/mol): 无可用
3、等张比容(90.2K):无可用
4、表面张力(dyne/cm):无可用
5、极化率:无可用
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:3
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积52.5
7.重原子数量:4
8.表面电荷:0
9.复杂度:13.5
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:2
性质与稳定性
1.有氧化性,与有机物接触能燃烧和爆炸,并放出有毒和刺激性的过氧化氮和氧化氮的气体。
2.易潮解,在空气中可被氧化成硝酸钠。本品是食品添加剂中急性毒性较强的物质之一,摄入大剂量的亚硝酸钠,可使血红蛋白变成高铁血红蛋白而失去输氧能力,造成身体组织缺氧,直至死亡。
3.吸湿性很强。常温下在空气中氧化极为缓慢,加热至320℃以上分解释放出氮气、氧气、一氧化氮,最终生成氧化钠。与有机物接触易燃烧和爆炸。晶体亚硝酸钠在160~162℃间有一转化点,此时膨胀性,导电性、比热和压电性等物理性质均发生变化。易溶于水和液氨,其水溶液呈碱性(PH=9)。微溶于无水乙醇、甲醇、乙醚。露置于空气中缓慢氧化成硝酸钠。加热到320 ℃以上分解放出氧气、氧化氮,最终生成氧化钠。与有机物接触易燃烧和爆炸。有毒!
4.易吸水,应保存于干燥密封的容器中,在空气中亚硝酸盐很容易被氧气氧化。NaNO2溶液很不稳定,不能长时间保存。NaNO2遇酸会形成弱酸,并产生棕色气体N2O3。亚硝酸钠有毒,不能用口尝。
5.NaNO2遇到不同的无机酸或羧酸会产生HNO2,在大多数的有机合成中,NaNO2都是以不稳定的HNO2形式参与反应的,而涉及到HNO2的反应通常很复杂,因为在溶液中还存在N2O3、ON+等。包括NOX、RNH2在内的一系列化合物都能发生重氮化和亚硝基化反应。
与氨及相关物质的反应 通常情况下,NaNO2的HCl溶液与氨反应能很快进行,而且多数下能定量反应。对伯胺而言,反应产生重氮离子中间体,然后消除一分子的N2形成碳正离子,再进一步与亲电试剂反应 (式1)[1~3]。
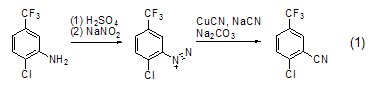
而当分子中存在多个亲核官能团时,所形成的重氮基团则可能继续反应 (式2)[4],在NaNO2作用下,伯胺首先形成重氮盐,然后与仲胺发生关环反应。

C-亚硝化反应 烷烃的中心碳一般不发生亚硝化反应,除非连有酰基、芳酰基、羰基、羧基、硝基、氰基、亚氨基或苯基等吸电子基团。一般的产物是亚硝胺或肟,硝基的邻位碳在NaNO2作用下生成肟 (式3)[5]。式4则是碳原子部位发生亚硝化,产物为亚硝胺[6]。

用NaNO2的HCl溶液对酚进行亚硝化会得到相应的亚硝基化合物。例如,苯酚一般生成4-亚硝基苯酚,同时会有少量2-取代的异构体 (约10%),而2-萘酚则会生成1-亚硝基-2-萘酚。如果用NaNO2与NaOH先作用后再加入乙酸,则可以在芳香环上直接引入亚硝基 (式5)[7]。
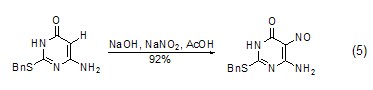
N-亚硝化 NaNO2除了可使碳原子发生亚硝化,也可使氮原子发生亚硝化,在加热条件下,产物可脱去一分子氮气而转化为酯类化合物 (式6)[8]。
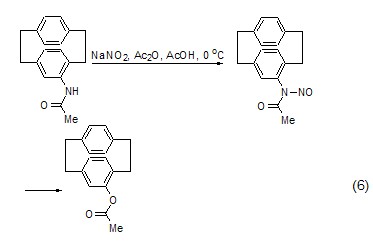
氧化反应 在催化剂等的作用下,NaNO2可将伯醇、仲醇等化合物氧化为相应的醛、酮 (式7)[9]。
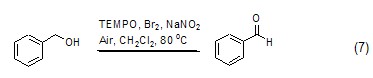
除了可以发生氧化反应以外,NaNO2同样可以参与还原反应,如亚硝酸根能够转化为硝酸根,进而实现对某些化合物的还原[10]。
6.稳定性[22] 稳定
7.禁配物[23] 强还原剂、活性金属粉末、强酸、铵盐、可燃物粉末或氰化物
8.避免接触的条件[24] 受热
9.聚合危害[25] 不聚合
10.分解产物[26] 氮氧化物
贮存方法
储存注意事项[27] 储存于阴凉、干燥、通风良好的专用库房内,远离火种、热源。库温不超过30℃,相对湿度不超过75%。包装要求密封,不可与空气接触。应与还原剂、活性金属粉末、酸类、食用化学品分开存放,切忌混储。储区应备有合适的材料收容泄露物。
合成方法
1.使氨气氧化产生氧化氮气体,用氢氧化钠或碳酸钠溶液吸收。
用铅还原硝酸钠,加热熔化硝酸钠,加少量金属铅,搅拌并继续加热至铅全部氧化。生成的块状物边冷却边分成小块,用热水萃取生成的氧化铅数次。通入二氧化碳气体使生成碳酸铅沉淀,经过滤,用稀硝酸准确中和滤液后,蒸发、浓缩析出亚硝酸钠结晶。经吸滤,用乙醇洗涤后干燥,再重结晶精制而得。
2.用烧碱溶液或纯碱吸收硝酸或硝酸盐生产中排出的含有少量NO和NO2的尾气,尾气中NO/NO2的比例要调节至使中和液中NaNO2与NaNO3的质量之比在8以下,在吸收过程中中和液应避免出现酸性,以免腐蚀设备。当中和液的相对密度为1.24~1.25,纯碱含量为3~5g/L时送去蒸发,在132℃时吸收液蒸发浓缩,然后冷至75℃,析出亚硝酸钠呈结晶,再经分离、干燥即得产品。反应方程式如下:

3.将硝酸合硝酸盐生产时排除的尾气中的一氧化氮合二氧化氮,用纯碱或烧碱溶液吸收而得中和液,经蒸发、结晶,然后利用亚硝酸钠与硝酸钠在水中的溶解度不同而将二者分离,即得成品。
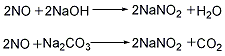
4.将42.5g硝酸钠与100g金属铅在瓷(或铁)坩埚中熔融搅拌,冷却后用200mL热水抽提,通入CO2数分钟,以沉淀溶于水中的氧化铅,铁离子等。过滤,滤液用稀硝酸酸化后,蒸发浓缩至干。然后加200~250mL乙醇在残渣上煮沸,过滤滤液以除去少量的硝酸钠,蒸馏滤液除去乙醇,则得到白色粉末,亚硝酸钠约20g。
提纯方法:将100g亚硝酸钠在70~80℃下溶于100mL水中,加入1~2g纯氢氧化钠以沉淀铁,冷却过滤,蒸发结晶,二次再结晶纯度更高,产量为75g。
5.采用吸收法。将稀硝酸生产过程中排出的尾气中一氧化氮和二氧化氨的比例调节到使中和液的亚硝酸和硝酸钠的质量比在8以下。然后将尾气自吸收塔底部通入,纯碱溶液从吸收塔的顶部喷淋吸收气体中的氧化氮,生成中和液。当中和液的相对密度为1.24~1.25、碳酸钠含量为3~5g/l时,进行蒸发浓缩、冷却结晶50~70℃析出亚硝酸钠结晶,再经离心分离,制得亚硝酸钠成品。其反应式如下。
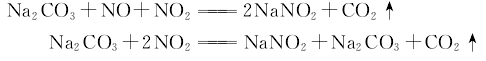
经离心分离出的母液,用作生产硝酸钠的原料。
6.将1份工业品亚硝酸钠溶解在1.5~2.0份70~80℃的纯水中。添加固体试剂氢氧化钠,调节PH值为12,静置沉淀,然后过滤。滤液蒸发到密度为1.45时再过滤,滤液冷却到室温,析出的亚硝酸钠晶体,用布氏漏斗抽滤,并不断搅拌,用少量冷水洗涤,然后移入磨口瓶中。母液可再蒸发结晶而得到大量亚硝酸钠,但需进行重结晶。
7.在氢氧化钠醇溶液中加入亚硝酸乙酯,放置二天,进行如下反应:
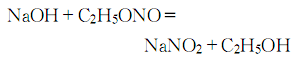
挥发物质,剩余物滤出(亚硝酸钠含量高达91%~96%)后在水中进行重结晶,可得亚硝酸钠含量95.5% ~99.8%。
用途
1.用作普通分析试剂、氧化剂和重氮化试剂,还用于亚硝酸盐和亚硝基化合物的合成,食品添加剂(有毒,限量使用)。
2.用作媒染剂、漂白剂、金属热处理剂、电镀缓蚀剂,医药上用作器械消毒剂、防腐剂等。
3.用于冰染染料、硫化染料、直接染料、酸性染料、分散染料、碱性染料、助染剂、H发孔剂的生产。也用于生产氨基偶氮苯、对位氨基苯酚等中间体。还用于有机颜料生产,如银珠R、鲜艳大红、大红粉、烛红、甲苯胺紫红、猩红色淀、立索尔大红、紫酱色淀CK等。医药工业用于制造乙胺嘧啶、氨基吡啉等。用于生产香兰素。用作丝绸和亚麻的漂白。织物染色的媒染剂。还用于金属热处理和电镀缓蚀剂。用于切削油、润滑油、抗冻液、液压系统。
4.肉类制品加工中用作发色剂,可用于肉类罐头、肉类制品。在肉制品中对抑制微生物的增殖有一定作用(对肉毒梭状芽孢杆菌有特殊抑制作用),能提高腌肉的风味。
5.用作丁二烯与苯乙烯乳液共聚的终止剂之一。也用作织物染色的媒染剂,丝绸、亚麻的漂白剂,金属热处理剂,电镀缓蚀剂,医药上利血管扩张剂及化学分析试剂以及制造亚硝酸钾、硝基化合物、偶氮染料等的原料。
6.解毒药。治疗氰化物中毒的解毒过程与亚甲蓝同,但作用较亚甲蓝强。
7.用作丁二烯与苯乙烯乳液共聚的终止剂。还可用作织物染色的媒染剂,丝绸、亚麻的漂白剂,金属热处理剂,电镀缓蚀剂,医药上作血管扩张剂及化学分析试剂,以及制造亚硝酸钾、硝基化合物、偶氮染料等的原料。
8.用于冰染染料、硫化染料、直接染料、酸性染料、分散染料、碱性染料、助染剂。也用于生产对位氨基苯酚等中间体。还用于有机颜料生产,如银珠R、鲜艳大红、大红粉、烛红、甲苯胺紫红、猩红色淀、立索尔大红及紫酱色淀CK等。医药工业用于制造乙胺嘧啶、氨基比林等。用于生产香兰素。用于丝绸和亚麻的漂白,织物染色的媒染剂。还用于金属热处理和电镀缓蚀剂。用于切削油、润滑油、抗冻液及液压系统。
9.用作水溶性胶黏剂和胶黏剂乳液的防腐剂。也用作制造硝基化合物、己内酰胺、偶氮染料、对氨基苯酚、硫化促进剂及香兰素等的原料。医药上用于制造安乃近、氨茶碱、乙胺嘧啶及咖啡因等药物。农药工业中用于制造辛硫磷、杀螟松及退菌特等杀虫剂。印染工业中用作棉纤维制品染色或印花的显色剂、纳夫妥染料染色的重氮化剂及拔染印花时底色保护剂。还用作丝绸、棉、麻漂白剂及丁烯氧化脱氢制丁二烯的精馏系统阻聚剂、电镀缓蚀剂、金属热处理剂及抗冻剂等。食品级亚硝酸钠用作食品添加剂时,最大使用量为0.15g/kg。残留量:肉类罐头≤0.05g/kg,肉制品≤0.03g/kg。
10.用于染料、医药工业制造染料和药物,也用于有机合成。[28]
安全信息
危险运输编码:暂无
危险品标志: 有毒
有毒  氧化剂
氧化剂  危害环境
危害环境
文献
1. Nielsen, M. A.; Nielsen, M. K.; Pittelkow, T. Org. Proc. Res. Dev., 2004, 8, 1059. 2. Siegrist, U.; Rapold, T.; Blaser, H.-U. Org. Proc. Res. Dev., 2003, 7, 429. 3. Jones, T. V.; Blatchly, R. A.; Tew, G. N. Org. Lett., 2003, 5, 3297. 4. Seela, F.; Lindner, M.; Glacüon, V.; Lin, W. J. Org. Chem., 2004, 69, 4695. 5. Matt, C.; Wagner, A.; Mioskowski, C. J. Org. Chem., 1997, 62, 234. 6. Hall, M. J.; McDonnell, S. O.; Killoran, J.; O’Shea, D. F. J. Org. Chem., 2005, 70, 5571. 7. Taddei, D.; Slawin, A. M.; Woollins, J. D. Eur. J. Org. Chem., 2005, 5, 939. 8. Glatzhofer, D. T.; Roy, R. R.; Cossey, K. N. Org. Lett., 2002, 4, 2349. 9. Liu, R.; Liang, X.; Dong, C.; Hu, X. J. Am. Chem. Soc., 2004, 126, 4112. 10. Sviridenko, F. B.; Stass, D. V.; Kobzeva, T. V.; Tretyakov, E. V.; Klyatskaya, S. V.; Mshvidobadze, E. V.; Vasilevsky, S. F.; Molin, Y. N. J. Am. Chem. Soc., 2004, 126, 2807. [1~10]参考书:现代有机合成试剂<性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7 [11~28]参考书:危险化学品安全技术全书.第一卷/张海峰主编.—2版.北京;化学工业出版社,2007.6 ISBN 978-7-122-00165-8
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号