| 物竞编号 | 0WCB |
|---|---|
| 分子式 | C38H69NO13 |
| 分子量 | 747.95 |
| 标签 | 甲氧基红霉素, 甲基红霉素, 克拉红霉素, 克拉仙霉素, Zecalar, Naxy, Macladin, 大环内酯类抗生素 |
编号系统
CAS号:81103-11-9
MDL号:暂无
EINECS号:暂无
RTECS号:KF4997000
BRN号:暂无
PubChem号:KF4997000
物性数据
1. 性状:无臭,味苦的白色结晶性粉末或无色针状结晶.
2. 密度(g/mL25 ºC):不确定
3. 相对蒸汽密度(g/mL,空气=1):未确定
4. 熔点(ºC):从氯仿一异丙醚(1:2)得无色针状结晶,熔点217~220℃(分解);或从乙醇结晶,熔点222~225℃
5. 沸点(ºC,常压):未确定
6. 沸点(ºC0.35mmHg):未确定
7. 折射率:-92 ° (C=1, CHCl3)
8. 闪点(ºC):未确定
9. 比旋光度(º):。[α]{D24-90.4°(C=1,氯仿)。
10. 自燃点或引燃温度(ºC):未确定
11. 蒸气压(kPa,):未确定
12. 饱和蒸气压(kPa,60ºC):未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(正辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:较易溶于氯仿或丙酮,微溶于乙醇,乙醚或甲醇,几不溶于水
毒理学数据
急性毒性LD50雄、雌小鼠,雄、雌大鼠(mg/kg):2740,2700,3470,2700口服;1030.850,669,753腹腔注射。
生态学数据
暂无
分子结构数据
暂无
计算化学数据
1、 疏水参数计算参考值(XlogP):3.2
2、 氢键供体数量:4
3、 氢键受体数量:14
4、 可旋转化学键数量:8
5、 互变异构体数量:3
6、 拓扑分子极性表面积(TPSA):183
7、 重原子数量:52
8、 表面电荷:0
9、 复杂度:1190
10、同位素原子数量:0
11、确定原子立构中心数量:18
12、不确定原子立构中心数量:0
13、确定化学键立构中心数量:0
14、不确定化学键立构中心数量:0
15、共价键单元数量:1
性质与稳定性
暂无
贮存方法
合成方法
1.以红霉素为原料,水解脱去氨基上的一个甲基,再和氯甲酸苄酯反应,对5位侧链四氢吡喃环上的羟基和氨基进行保护,然后在二甲亚砜和四氢呋喃中和碘甲烷反应,对6位上的羟基进行甲基化,再催化氢解脱去保护基,和甲醛反应对氨基进行羟甲基化,最后还原为甲基,即为克拉霉素。

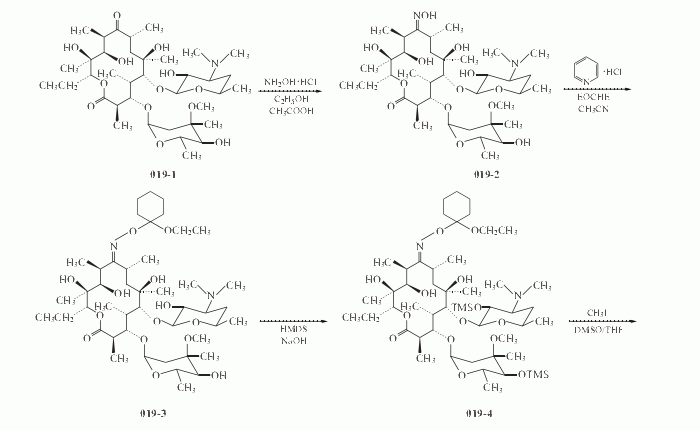
2.(1)红霉素A肟(019-2)的制备
在反应瓶中加入无水乙醇50ml和红霉素(019-1)10.0g(13.6mmol),搅拌下滴加冰醋酸,溶液呈透明后,加入盐酸羟胺7.0g(100.0mmol),在适当的酸碱缓冲体系下,升温至50~60 ºC ,搅拌反应8~24h.TLC跟踪确认反应达终点后,终止反应.冷至室温,过滤除去无机盐,滤液减压蒸发至干,得白色固体.将该固体溶于20ml乙酸乙酯中,搅拌下加入4mol/L NaOH溶液,调至pH>=12.静置分层,有机层用适量水洗涤2~3次后,真空浓缩至干,得白色固体,干燥至恒重,得019-2 9.98g,收率99.9%.含019-2 93.5%,其中E-肟 82.9%,Z-肟10.6%,红霉素降解产物红霉素A 8,9-脱水-6,9-半缩酮<=2%(HPLC法).将019-2重结晶得019-2.纯品,收率95.6%。
(2)2’,4”-O-双(三甲基硅)红霉素A 9-O-(1-乙氧基环己基)肟[2’,4’’-Obis(trimethylsilyl)-eryth-romycin A 9-O91-ethoxycyclohexyl]oxime](019-4)的制备
在反应瓶中加入乙腈500ml、019-2 50.0g(67mmol)和盐酸吡啶15.0g(134mmol),搅拌下加
入1-乙氧基环己烯(EOCHE)30.0ml(223mmol),在室温(28 ºC)下搅拌反应,反应液逐渐变清无色,3h后全部转化为红霉素A9-O-(1-乙氧基环己基)肟(019-3),再加入1,1,1,3,3,3-六甲基二硅氨烷(HMDS)50.0ml(240mmol),反应液立即呈白色浊态.搅拌反应2h后,加入4mol/L NaOH溶液调至PH>=10,用乙酸乙酯(200ml*2)提取,有机相用水洗,饱和食盐水洗,无水MgSO4干燥过夜.过滤,滤液减压蒸除溶剂得019-4,mp108~110 ºC.
(3)2’,4’’-O-双(三甲基硅)6-O-甲基红霉素A 9-O-(1-乙氧基环己基)肟[2’,4’’-Obis(trimethylsilyl)-6-O-methylerythromycin A 9-O-(1-ethoxycyclohexyl)oxime](019-5)的制备。
在反应瓶中加入DMSO/THF(体积比1:1)400ml和019-4(上步一批量),搅拌溶解,再加入碘甲6.0ml(96mmol)和82%的KOH粉末6.0g(88mmol),于0 ºC 搅拌反应1h.加水200ml,用乙酸乙酯提取(200ml*2),无水MgSO4干燥有机相,过滤,滤液蒸除溶剂得019-5,mp127~129 ºC .直接用于下步反应.
(4)克拉霉素(019)的合成
在反应瓶中加入250ml乙醇和水,再加入019-5(上步一批得量),搅拌溶解,搅拌下加入甲酸5.0ml(132mmol),反应数小时后,TLC跟踪显示得6-O-甲基红霉素A 9-O-(1-乙氧基环己基)肟和6-O-甲基红霉素 A-9-肟,再补加NaHSO3 50.0g(480mmol),搅拌加热至回流,反应2h.用4mol/L的NaOH溶液调至PH>=10,析出白色固体019,用乙醇重结晶得精品019 24.7g,以红霉素A计总收率达49.5%,mp222~225 ºC .

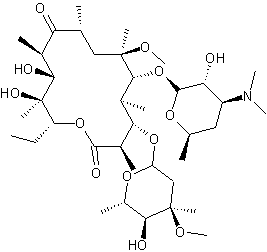
用途
1.大环内酯类抗生素,为红霉素的衍生物,把红霉素A的6位上的OH基改为OCH3,即为克拉霉素。对革兰阳性菌和阴性菌、衣原体以及分枝杆菌有效,几乎能有效地抑制所有呼吸系统病原菌。对胃酸稳定,口服吸收好,血药浓度高,血半衰期长。其用途和红霉素相似,对呼吸道、泌尿道、皮肤、耳鼻喉科等多种感染有效。属大环内酯类抗生素,用于治疗上、下呼吸道感染,皮下软组织感染等.
2.大环内酯类抗生素,为红霉素的衍生物。对革兰阳性菌,如金黄色葡萄球菌、链球菌、肺炎球菌等有抑制作用,对部分革兰阴性菌如流感嗜血杆菌、百日咳杆菌、淋病双球菌、嗜肺军团菌和部分厌氧菌,如脆弱拟杆菌、消化链球菌、痤疮丙酸杆菌等也有抑制作用.
安全信息
危险运输编码:暂无
危险品标志: 有害
有害
安全标识:S22
危险标识:暂无
文献
[1] Merck Index. 13th : 2362 [2] Morimoto S, et al. J Antibiot, 1984,37:187. [3] Fernandes P B ,et al.Antimicrob Ag Chemother1986,30:865. [4] 国外医药:抗生素分册,1996,17:33-37. [5] 王文梅。 中国医药工业杂志,1993,24:325-329. [6] Morimoto S.J Antibiot,1990,43:187-189. [7] EP,41355.1981. [8] US,4331803.1982. [9] Morimoto S,et al.J Antibiot,1990,43:295. [10]Sun J G,et al.J Org |Chem,2002,22:951.(中文) [11] Morimoto S,et al.J Antibiot,1990,43:544. [12] US,4672109.1987. [13]Watanabe Y,et al.J Antibiot,1993,46:647. [14] Omura S,et al.药学杂志,1992,112:593.(日文) [15] US,4990602.1991. [16] Watanabe Y,et al.J Antibiot,1993,46:1163 [17] 梁建华等。精细化工,2003,20:310. [18] 邓志华等。中国药物化学杂志,2003,13:87-89. [19] 梁建华等。有机化学,2003,23:841. [20] US,5719272.1998. [21] US,5864023.1999. [22] US,5837829.1998. [23] Allevi P,et al. Bioorg Med Chem,1999,7:2749. [24] US,6515116.2003. [25] 梁建华等,有机化学,2005,25:438-441 [1] Merck Index. 13th : 2362 [2] Morimoto S, et al. J Antibiot, 1984,37:187. [3] Fernandes P B ,et al.Antimicrob Ag Chemother1986,30:865. [4] 国外医药:抗生素分册,1996,17:33-37. [5] 王文梅。 中国医药工业杂志,1993,24:325-329. [6] Morimoto S.J Antibiot,1990,43:187-189. [7] EP,41355.1981. [8] US,4331803.1982. [9] Morimoto S,et al.J Antibiot,1990,43:295. [10]Sun J G,et al.J Org |Chem,2002,22:951.(中文) [11] Morimoto S,et al.J Antibiot,1990,43:544. [12] US,4672109.1987. [13]Watanabe Y,et al.J Antibiot,1993,46:647. [14] Omura S,et al.药学杂志,1992,112:593.(日文) [15] US,4990602.1991. [16] Watanabe Y,et al.J Antibiot,1993,46:1163 [17] 梁建华等。精细化工,2003,20:310. [18] 邓志华等。中国药物化学杂志,2003,13:87-89. [19] 梁建华等。有机化学,2003,23:841. [20] US,5719272.1998. [21] US,5864023.1999. [22] US,5837829.1998. [23] Allevi P,et al. Bioorg Med Chem,1999,7:2749. [24] US,6515116.2003. [25] 梁建华等,有机化学,2005,25:438-441 [1] Merck Index. 13th : 2362 [2] Morimoto S, et al. J Antibiot, 1984,37:187. [3] Fernandes P B ,et al.Antimicrob Ag Chemother1986,30:865. [4] 国外医药:抗生素分册,1996,17:33-37. [5] 王文梅。 中国医药工业杂志,1993,24:325-329. [6] Morimoto S.J Antibiot,1990,43:187-189. [7] EP,41355.1981. [8] US,4331803.1982. [9] Morimoto S,et al.J Antibiot,1990,43:295. [10]Sun J G,et al.J Org |Chem,2002,22:951.(中文) [11] Morimoto S,et al.J Antibiot,1990,43:544. [12] US,4672109.1987. [13]Watanabe Y,et al.J Antibiot,1993,46:647. [14] Omura S,et al.药学杂志,1992,112:593.(日文) [15] US,4990602.1991. [16] Watanabe Y,et al.J Antibiot,1993,46:1163 [17] 梁建华等。精细化工,2003,20:310. [18] 邓志华等。中国药物化学杂志,2003,13:87-89. [19] 梁建华等。有机化学,2003,23:841. [20] US,5719272.1998. [21] US,5864023.1999. [22] US,5837829.1998. [23] Allevi P,et al. Bioorg Med Chem,1999,7:2749. [24] US,6515116.2003. [25] 梁建华等,有机化学,2005,25:438-441
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号