| 物竞编号 | 03VA |
|---|---|
| 分子式 | C4H6CuO4 |
| 分子量 | 181.63 |
| 标签 | 乙酸铜, 无水乙酸铜, Cupric acetate, 氧化剂 |
编号系统
CAS号:142-71-2
MDL号:MFCD00008690
EINECS号:205-553-3
RTECS号:AG3480000
BRN号:暂无
PubChem号:24882058
物性数据
1.性状:蓝色晶体
2.密度(g/mL,25/4℃):1.93
3.熔点(ºC):130~140
4.溶解性:溶于水(6.79 g/100 mL,25 oC)以及醋酸、吡啶,不溶于乙醚。
毒理学数据
1、急性毒性:
大鼠经口LD50:501 mg/kg;
大鼠腹腔LD50:14700 ug/kg;
大鼠皮下LD50:350 mg/kg;
大鼠静脉LD50:17100 ug/kg;
小鼠经口LD50:196 mg/kg;
小鼠腹腔LD50:2500 ug/kg;
小鼠静脉LD50:20 mg/kg。
2、 慢性毒性/致癌性
大鼠经口TDLo:23750 mg/kg/42W-C;
3、 生殖毒性:
大鼠经皮TDLo:40 mg/kg
生态学数据
1、其它有害作用:该物质对环境可能有危害,对水体应给予特别注意。
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:4
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积80.3
7.重原子数量:9
8.表面电荷:0
9.复杂度:25.5
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:3
性质与稳定性
1.常温常压下稳定。
2.禁配物:氧化剂、碱。
3.具有吸湿性,应在干燥处存放。对皮肤、眼睛和呼吸系统有刺激性。
贮存方法
常温干燥密封保存。
合成方法
1.将50g五水合硫酸铜溶于500ml水中,过滤,另取57g十水合碳酸钠溶于240ml水,加热至60℃,慢慢加入硫酸铜溶液,并不断搅拌。静置,滤出沉淀,用热水洗涤至无硫酸为止,将沉淀放在300ml水中,加入2ml氨水搅拌,静置,倾出上层溶液,如此洗涤、沉淀数次。在烧杯中加入180ml水,热至60℃,加入22g冰醋酸,然后加入上述洗好的碱式碳酸铜,直至容器底部略有剩余。过滤,滤液蒸发浓缩至原体积的1/3时,冷却,过滤,用2ml水洗涤,于室温干燥,得成品。母液继续蒸发,并在快出结晶时加入5ml25%乙酸,又可获得部分成品。其得32-35g。
2.将一水醋酸铜(Ⅱ)加热至105℃,或用一水醋酸铜与醋酸酐加热回流,冷却后过滤,将所得晶体放在置有固体氢氧化钾或浓硫酸的真空保干器中干燥。
3.无水醋酸铜可通过在90 oC加热或在醋酸酐溶液中回流然后乙醚洗涤制备而来。
用途
1.分析试剂,有机合成催化剂,杀虫剂、杀菌剂、印染固色剂,制备巴黎绿的中间体。用作色层分析试剂。
2.醋酸铜可以作为碳负离子、自由基和烃类化合物的氧化剂,可以实现电负性底物的氧化偶联反应和Si-C、Bi-C、Pb-C和Sb-C键的溶剂裂解反应。还能用于烯烃与重氮酯的环丙化反应。醋酸铜也可作为路易斯酸参与反应[1]。
醋酸铜对碳负离子具有氧化活性,在吡啶存在下能够实现端炔的氧化偶联反应得到二炔化合物 (式1~式4)[2]。
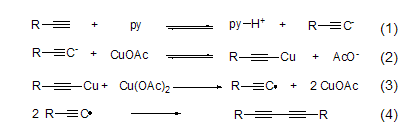
采用三氟甲基磺酸铜作氧化剂,可以实现α-磺酰基锂碳阴离子的自身偶联反应 (式5),但是采用醋酸铜作氧化剂,则可以将其氧化为α,β-不饱和砜化合物 (式6)[3]。其它碳阴离子也能在醋酸铜作用下发生偶联反应,如β-内酰胺的合成 (式7)[4]。
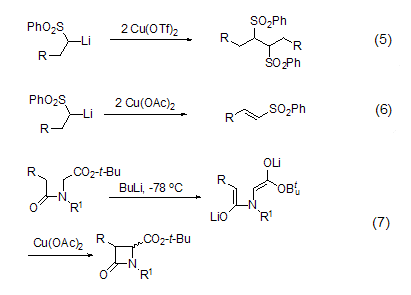
醋酸铜还能氧化烃类底物的C-H键。如苯酚的邻位羟基化反应可以被醋酸铜在氧气和吗啉存在下催化实现。当隔绝氧气时,定量醋酸铜在醋酸存在下则可以实现苯酚的邻位乙酸化反应 (式8)[5]。
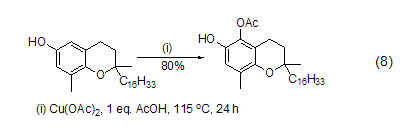
过氧酯在醋酸铜催化下可以作用于丙烯化合物发生烯丙基氢被酰氧基取代的反应 (式9)[6]。反应很可能是先形成了烯丙基自由基,然后与Cu(II)快速反应得到Cu(III)中间体,进而经历周环过渡态得到最终酰氧基取代烯烃。
在催化量的醋酸钯和过量醋酸铜共同作用下也能实现烯丙基氧化反应,如N-Boc-烯丙基胺分子内环化反应 (式10)[7]。
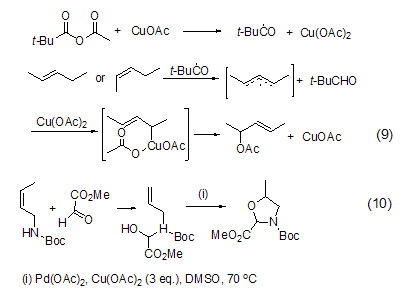
醋酸铜还能实现碳-金属键的氧化反应。在甲醇和氧气氛围下,催化量的醋酸铜可以促进乙烯基Si-C键的断裂得到乙烯基醚化合物 (式11)[8],反应具有高度的立体选择性,完全得到反式烯醇醚。在水存在下也能得到相应的醛。
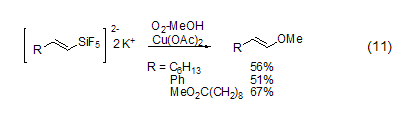
与自由基引发剂联合使用,醋酸铜还能参与自由基的氧化反应。如β-羰基酯在Mn(OAc)3氧化下得到自由基,然后经历分子内环化得到烷基自由基,进而在醋酸铜作用下被氧化为相应的烯烃 (式12)[9]。
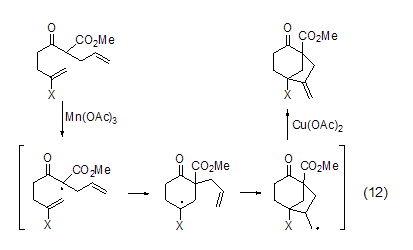
醋酸铜还能作为钯试剂催化反应的氧化剂,将还原后的钯试剂重新氧化为Pd(II),进而重新进入催化循环 (式13)[10]。此外,醋酸铜与手性亚胺配体结合能诱导烯烃与重氮乙酸酯的不对称环丙化反应 (式14)[11]。
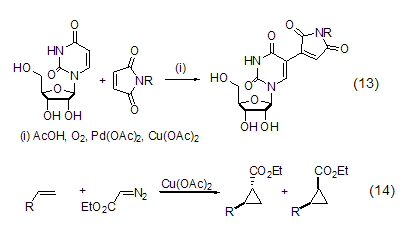
醋酸铜能与含氮化合物有效配位,因而能够作为路易斯酸参与含氮化合物的反应。如催化量的醋酸铜在氧气存在下可实现酰肼到羧酸的转换 (式15)[12]。
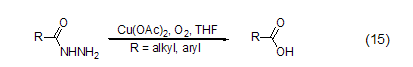
醋酸铜在氧气存在下还能催化苯乙炔与二甲基胺的偶联反应,得到N,N-二甲基-2-苯基乙炔胺化合物 (式16)[13]。该反应中氧气是一个关键因素,在没有氧气存在下,1,4-二苯基丁炔是唯一的偶联产物。

安全信息
危险运输编码:UN3077 9/PG 3
危险品标志: 有害
有害  危害环境
危害环境
文献
1. Heaney, H.; Christie, S. Science of Synthesis, 2004, 3, 305. 2. (a) Eglinton, G.; McCrae, W. Adv. Org. Chem., 1963, 4, 225. (b) Cresp, T. M.; Sondheimer, F. J. Am. Chem. Soc., 1975, 97, 4412. 3. Baudin, J.-B.; Julia, M.; Rolando, C.; Verpeaux, J.-N. Tetrahedron Lett., 1984, 25, 3203. 4. Kawabata, T.; Minami, T.; Hiyama, T. J. Org. Chem., 1992, 57, 1864. 5. Takizawa, Y.; Tateishi, A.; Sugiyama, J.; Yoshida, H.; Yoshihara, N. Chem. Commun., 1991, 107. 6. Beckwith, A. L. J.; Zavitsas, A. A. J. Am. Chem. Soc., 1986, 108, 8230. 7. Van Benthem, R. A. T. M.; Hiemstra, H.; Speckamp, W. N. J. Org. Chem., 1992, 57, 6082. 8. Yoshida, J.; Tamao, K.; Kakui, T.; Kurita, A.; Murata, M; Yamada, K.; Kumada, M. Organometallics, 1982, 1, 369. 9. Snider, B. B.; Zhang, Q.; Domobroski, M. A. J. Org. Chem., 1992, 57, 4195. 10. Itahara, T. Chem. Lett., 1986, 239. 11. Brunner, H.; Wutz, K. New. J. Chem., 1992, 16, 57. 12. Tsuji, J.; Nagashima, T.; Nguyen, T. Q.; Takayanagi, H. Tetrahedron, 1990, 36, 1311. 13. Peterson, L. Tetrahedron Lett., 1968, 51, 5357. 14.参考书:现代有机合成试剂<性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号