| 物竞编号 | 10P2 |
|---|---|
| 分子式 | C16H12N2O7 |
| 分子量 | 344.28 |
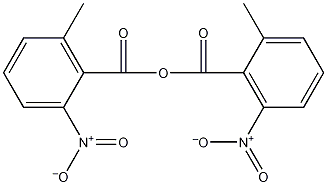
| 标签 | 6-硝基邻甲基酸酐, 6-Nitro-o-toluic Anhydride, MNBA, 脱水缩合剂 |
编号系统
CAS号:434935-69-0
MDL号:MFCD06797117
EINECS号:暂无
RTECS号:暂无
BRN号:暂无
PubChem号:24885612
物性数据
1.性状:极淡的黄色-红黄色晶体粉末
2.熔点(℃):177
毒理学数据
暂无
生态学数据
暂无
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):3.6
2.氢键供体数量:0
3.氢键受体数量:7
4.可旋转化学键数量:4
5.互变异构体数量:无
6.拓扑分子极性表面积135
7.重原子数量:25
8.表面电荷:0
9.复杂度:506
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
暂无
贮存方法
暂无
合成方法
暂无
用途
MNBA是一个非常有效的脱水缩合试剂,经过一个简单的步骤混合反应物试剂,然后从等摩尔的羧酸和醇类制备羧酸酯类,从羟基羧酸中制备内酯,反应产物收益率好,化学纯度高。
1.酯化反应
在碱性条件下,首先将三乙基胺,二甲基氨基吡啶(DMAP)和MNBA溶于溶剂中,混合后加入羧酸,室温下搅拌,加入醇厚,羧酸酯就可以很容易的获得1)。表格1中就是一个典型的例子,MNBA中的硝基基团在室温下促进酯化反应。此外,在MNBA的芳香环上2-位和6-位处引入取代基可以阻止羧酸酯副产物的生成。这两种效应使得反应活性增强,合成羧酸酯收益率高,纯度高。
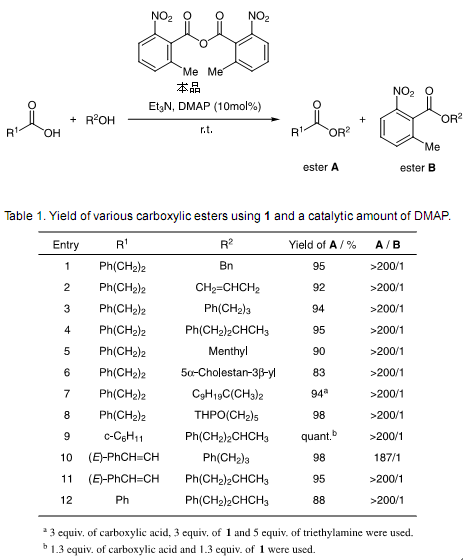
2.内酯化反应
Shiina等人利用MNBA进行分子内的酯化反应2),使用DMAP作为基质和催化剂制备大环酮类,收益率很高,选择性也很高。这个方法可以应用到具有酸敏结构的化合物比如说乙缩醛。此外,当化合物中含有ω-羟基羧酸,和二级羟基基团时(见表二)可以得到相应的内酯,选择性很高。这个方法被成功的应用到了合成八环乳糖 A(Scheme 1 )3)和八环乳糖 B4)的八元环结构上面。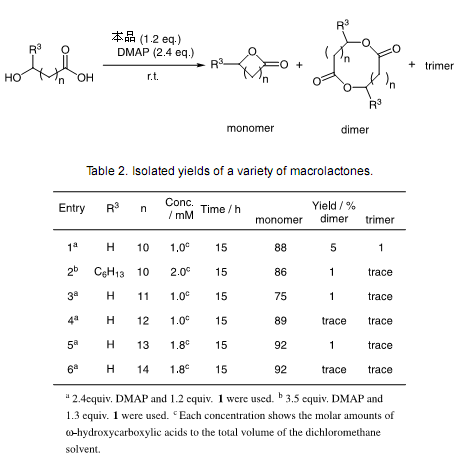
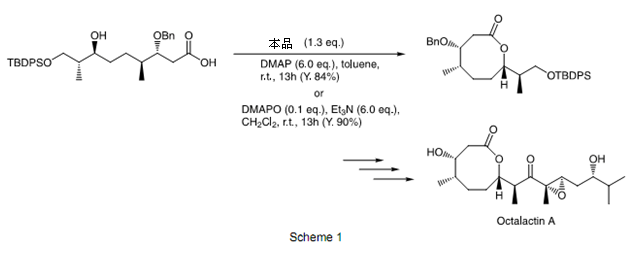
此外,使用三乙基胺作基质,4-二甲氨基吡啶氧化物(DMAPO)作催化剂进行内酯化反应式,MNBA,三乙基胺,4-二甲氨基吡啶氧化物溶解在溶剂里面,然后缓慢的逐滴滴加羟基羧酸,室温下搅拌,反应结束后得到相应的内酯。(Scheme 2)
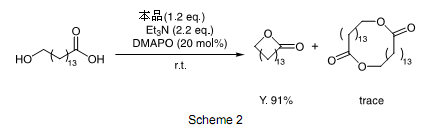
综上所述,使用产品MNBA的酯化反应和内酯化反应在碱性至中性的条件下都可以完成,另外,这个方法分离中间产物简单。总之,MNBA是一个非常有效的脱水缩合试剂,经过一个简单的步骤混合反应物试剂,然后从等摩尔的羧酸和醇类制备羧酸酯类,从羟基羧酸中制备内酯,反应产物收益率好,化学纯度高。
安全信息
危险运输编码:暂无
危险品标志: 刺激
刺激
安全标识:S26
危险标识:R36/37/38
文献
1)I. Shiina, R. Ibuka, M. Kubota, Chem. Lett., 2002, 286; N. Nishino, J. Synth. Org. Chem. Jpn., 2002, 60, 996; Tokyo Kasei Kogyo Jpn. Kokai Tokkyo koho 2003 335731, 2003. 2) I. Shiina, M. Kubota, R. Ibuka, Tetrahedron Lett., 2002, 43, 7535 . 3) I. Shiina, M. Hashizume, Y. Yamai, H. Oshiumi, T. Shimazaki, Y. Takasuna, R. Ibuka, Chem. Eur. J., 11, 6601 (2005). M-T. Dinh, S. Bouzbouz, J.-L. Peglion, J. Cossy, Synlett, 2005,2851. 4) I. Shiina, M. Kubota, H. Oshiumi, M. Hashizume, J. Org. Chem., 69, 1822 (2004). I. Shiina, M. Kubota, H. Oshiumi, M. Hashizume, Y. Yamai, R. Ibuka, Tetrahedron Lett., 45, 543 (2004).
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号