| 物竞编号 | 041P |
|---|---|
| 分子式 | C6H12N2 |
| 分子量 | 112.17 |
| 标签 | 1,4-二氮杂二环[2.2.2]辛烷, 1,4-乙烯哌嗪, 二环[2.2.2]-1,4-二氮杂辛烷, 二乙烯二胺, 三乙撑二胺, 三乙烯二胺(六水), 1,4-二叠氮双环[2.2.2]辛烷, 三乙基二胺, DABCO,TED,Triethylenedi-amine, 1,4-Diazabicyclo [2.2.2] octane, 1,4-vinyl-piperazine, bicyclo [2.2.2]-1,4-diaza-octane, 2-ethylene diamine, triethylene support diamine, three ethylene diamine (6 water), 1,4 - azido bicyclo [2.2.2] octane, triethylenediamine, 聚合催化剂, 石油添加剂 |
编号系统
CAS号:280-57-9
MDL号:MFCD00006689
EINECS号:205-999-9
RTECS号:HM0354200
BRN号:103618
PubChem号:24893714
物性数据
1. 性状:无色晶体
2. 熔点(℃):158~160
3. 溶解性:溶于水和大多数有机溶剂,可在多种有机溶剂中使用。
毒理学数据
刺激皮肤、黏膜、眼睛和呼吸道,能引起皮肤过敏和支气管哮喘。长期接触或吸入高浓度的气体能引起头痛、记忆力衰退等。操作现场最高允许浓度1mg/L。经口最大致死浓度(LD)1.8mg/kg体重。
生态学数据
碱性,其蒸气对眼睛、鼻孔、咽喉和呼吸器官有刺激性,是过敏原,可能引起过敏和哮喘,并能引起疼痛。
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):-0.2
2.氢键供体数量:0
3.氢键受体数量:2
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积6.5
7.重原子数量:8
8.表面电荷:0
9.复杂度:61.5
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
具有非常强的吸湿性,且在室温下就能升华,因而需要在低温 (< 5 oC) 和干燥条件下储存,在通风橱中操作和使用。
1,4-二氮杂双环[2.2.2]辛烷 (DABCO) 在有机合成中主要被用作一个功能特殊的有机碱。它的环状结构不仅使得氮原子上的孤对电子更加裸露,具有较强的碱性,而且使得分子具有较强刚性的位阻。
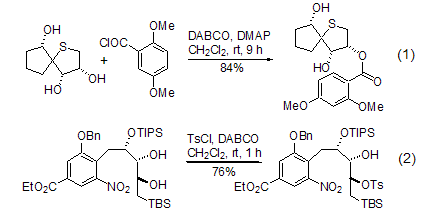
DABCO可以作为一个正常的有机胺用于碱催化的有机反应[1~5]。例如:卤代烃与醇生成醚的反应、磺酰氯与醇生成磺酸酯的反应或者酰氯与醇生成羧酸酯的反应等。但是,在这些反应中使用DABCO不仅可以提高反应的产率,而且显示出非常明显的区域选择性 (式1,式2)[4,5]。
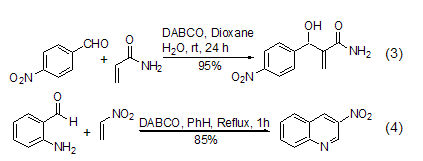
DABCO一个非常独特的用途是作为有机碱催化Baylis-Hillman 反应[6~9]。虽然其它有机碱也可以催化该反应,但是DABCO具有最为普遍的应用范围。最近文献报道,苯甲醛与丙烯酰胺在DABCO催化下进行的Baylis-Hillman 反应可以在含水体系中进行,这是一个很有意义的结果 (式3)[8]。如果反应底物结构合适的话,可以通过Baylis-Hillman反应直接制备含氮杂环化合物 (式4)[9]。
DABCO另一个独特的用途是作为有机碱用于金属钯或者镍催化的芳基氟磺酸酯与二苯基氢化膦的取代反应,可以高产率地得到相应的二苯基膦芳烃化合物。该反应用于制备手性二苯基膦芳烃化合物作为金属不对称催化反应的手性配体时具有重要的应用价值 (式5)[10,11]。
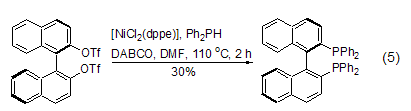
此外,DABCO还可以与多种有机化合物和金属有机化合物生成结构确定和物化性质稳定的分子复合物[12,13]。例如:将三甲基铝与DABCO在乙醚中回流,可以得到2:1的晶体分子复合物 (式6)[14,15]。这样的三甲基铝复合物不仅可以在正常的实验条件下操作,而且反应活性也更容易控制。
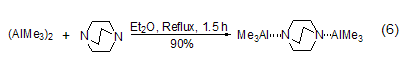
贮存方法
应密封储存,存放于阴凉通风处。防潮、防热,与酸类物品隔离。贮存于阴凉、干燥的库房内。
合成方法
1、将1,2-二氯乙烷和氨水送入管式反应器中,于150-250℃、392kPa压力下进和热压氨化反应。反应液以碱中和得到混合游离胺,经浓缩除去氯化钠,然后将粗吕减压蒸馏,收集不同馏分进行分离。在获得该品同时,并联产乙二胺、二亚乙基三胺、三亚乙基四胺、四亚乙基五胺和多亚乙基多胺。从生产六水哌嗪的母液中经分馏可得该品,第生产100t六水哌嗪可得六水三亚乙基二胺约3-4t。

2、由N-羟乙基哌嗪合成TEDA在内径为24cm的固定床反应器中添入40-60ml的BaSr2型催化剂(钡锶质量比为3.6:1),升温至设定温度,用计量泵输入40%-60%的原料水溶液,原料气空速为615-219h,粗羟乙基哌嗪进入反应器经预热汽化后与催化剂床层接触反应。合成三乙烯二胺的工艺条件为:反应温度为355-370℃,N-羟乙基哌嗪水溶液的含量为60%(质量分数),原料气空速为20000h,催化剂颗粒直径为2mm。在此条件下,粗羟乙基哌嗪的转化率为100%,三乙烯二胺的选择为90%,纯度达99%以上。
从生产六水哌嗪的母液中经分馏也可得到本品。
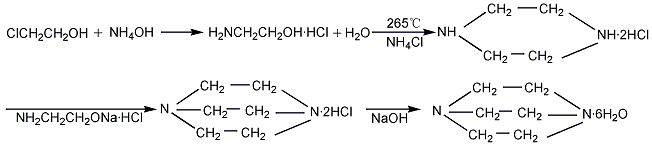
3、以羟乙基哌嗪或双羟乙基哌嗪为原料,在催化剂作用下,高温进行环化反应,制取三亚乙基二胺。
4、二氯乙烷和氨水进行热压氨解反应,反应液用碱中和,得混合游离胺,再经浓缩,同时除去副产物氯化钠,然后将粗品进行减压精馏,即可得成品。或者在生产六水哌嗪时经分馏可得三乙烯二胺。
5、以乙二胺或乙醇胺、二乙醇胺或二乙烯三胺为原料制取时,只能达到中等程度的产率。例如,二乙烯三胺在常压和360℃的温度下,以86%二氧化硅和12%氧化铝组成的催化剂进行反应,可以制得同等产量的哌嗪、烷基哌嗪、吡嗪以及乙二胺和除了双环化合物之外的同系物。再经蒸馏,以丙酮再结晶和石
油醚洗涤,即可得到纯度为95%的三乙烯二胺,再经升华处理后纯度可以达到98%。
6、以羟乙基哌嗪或双羟乙基哌嗪为原料,在高温下进行环化反应,制取三乙烯二胺。所用催化剂有氧化铝、活性白土、磷酸锆等。例如,将羟乙基哌嗪通过内装煅烧过APO-9( 由磷酸与勃姆石反应的产物)催化剂的反应管,控制管内反应温度在400℃,可制得三乙烯二胺,产率在81.4%。
用途
1. 用作聚氨酯的催化剂,因室温时是结晶固体,直接使用有困难,必须先将其溶解于相应的溶剂配成溶液,如乙二醇、丙二醇等。应当指出,若以六结晶水三乙烯二胺配制溶液时,必须将其中水分用真空减压蒸馏法脱除。亦用于油添加剂。
2. 用作制取聚氨酯类泡沫塑料的催化剂和石油添加剂。
3.在锅炉水处理中用作缓蚀剂。还用作聚氨酯发泡和聚合的催化剂,环氧树脂固化的促进剂,丙烯腈、乙烯和烷乙烯氧化物的催化剂。
4.非亲核碱。分裂β一酮酸醋和偕二醋及脱卤化氢反应的试剂。环化催化剂。制备氨基甲酸酯泡沫的催化剂。与溴的络合物用于氧化芳香醇和仲醇。与有机镁、锂、锌的化合物形成络合物,以增大活性并参与许多反应。
安全信息
危险运输编码:UN1325 4.1/PG 2
危险品标志: 易燃
易燃  有害
有害
安全标识:S3 S16 S26 S60 S36/S37 S37/S39
危险标识:R11 R22 R41 R36/37/38 R36/38 R52/53
文献
1. Wanner, M. J.; Koch, M.; Koomen, G.-J. J. Med. Chem., 2004, 47, 6875. 2. Dong, S.; Paquette, L. A. J. Org. Chem., 2005, 70, 1580. 3. Nelson, T. D.; Rosen, J. D.; Smitrovich, J. H.; Payack, J.; Craig, B.; Matty, L.; Huffman, M. A.; McNamara, J. Org. Lett., 2005, 7, 55. 4. Paquette, L. A.; Dong, S. J. Org. Chem., 2005, 70, 5655. 5. Suzuki, M.; Kambe, M.; Tokuyama, H.; Fukuyama, T. J. Org. Chem., 2004, 69, 2831. 6. Declerck, V.; Ribiere, P.; Martinez, J.; Lamaty, F. J. Org. Chem., 2004, 69, 8372. 7. Clive, D. L. J.; Yu, M.; Li, Z. Chem. Commun., 2005, 906. 8. Yu, C.; Hu, L. J. Org. Chem., 2002, 67, 219. 9. Yan, M.-C.; Tu, Z.; Lin, C.; Ko, S.; Hsu, J.; Yao, C.-F. J. Org. Chem., 2004, 69, 1565. 10. Hope, Eric G.; Stuart, Alison M.; West, Andrew J. Green Chem., 2004, 6, 345. 11. Botman, P. N. M.; Fraanje, J.; Goubitz, K.; Peschar, R.; Verhoeven, J. W.; Van Maarseveen, J. H.; Hiemstra, H. Adv. Synth. Catal., 2004, 346, 743. 12. Dybtsev, D. N.; Chun, H.; Kim, K. Angew. Chem. Int. Ed., 2004, 43, 5033. 13. Cardillo, P.; Corradi, E.; Lunghi, A.; Meille, S. V.; Messina, M. T.; Metrangolo, P.; Resnati, G. Tetrahedron, 2000, 56, 5535. 14. Bradford, A. M., Bradley, D. C., Hursthouse, M. B., Motevalli, M. Organometallics, 1992, 11, 111. 15. Biswas, K.; Prieto, O.; Goldsmith, P. J.; Woodward, S. Angew. Chem. Int. Ed., 2005, 44, 2232. 16.参考书:现代有机合成试剂<性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无

![1,4-二氮杂二环[2.2.2]辛烷结构式](http://staticv5.basechem.org/img/tupu/old/bf2d4a78df9d46c596c800c0bba69e6b.gif)



 沪公网安备 31010602001115号
沪公网安备 31010602001115号