| 物竞编号 | 173P |
|---|---|
| 分子式 | N2 |
| 分子量 | 28.01 |
| 标签 | 冷冻剂 |
编号系统
CAS号:7727-37-9
MDL号:MFCD00011416
EINECS号:231-783-9
RTECS号:QW9700000
BRN号:暂无
PubChem号:暂无
物性数据
1.性状:无色无味压缩气体[1]
2.熔点(℃):-209.9[2]
3.沸点(℃):-196[3]
4.相对密度(水=1):0.81(-196℃)[4]
5.相对蒸气密度(空气=1):0.97[5]
6.饱和蒸气压(kPa):1026.42(-173℃)[6]
7.临界温度(℃):147.1[7]
8.临界压力(MPa):3.40[8]
9.辛醇/水分配系数:0.67[9]
10.溶解性:微溶于水、乙醇,溶于液氨。[10]
毒理学数据
1.急性毒性 暂无资料
2.刺激性 暂无资料
生态学数据
1.生态毒性 暂无资料
2.生物降解性 暂无资料
3.非生物降解性 暂无资料
分子结构数据
1、摩尔折射率:3.87
2、摩尔体积(cm3/mol):31.9
3、等张比容(90.2K):70.5
4、表面张力(dyne/cm):23.6
5、极化率(10-24cm3):1.53
计算化学数据
1.疏水参数计算参考值(XlogP):0.1
2.氢键供体数量:0
3.氢键受体数量:2
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积47.6
7.重原子数量:2
8.表面电荷:0
9.复杂度:8
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.常温下化学性质稳定,加热至560℃时,能被镁、钙、锂和另外一些金属所吸收。在更高温度下能直接与氧和氢化合。溶于水(0℃时2.33cm3/100ml水,40℃时1.42cm3/100ml水),微溶于醇。液化温度77.35k,固化温度63.2k。无色无嗅的气体,在水中的溶解度很小,在室温下化学性质为惰性,但可被碳吸收。
2.稳定性[11] 稳定
3.聚合危害[12] 不聚合
贮存方法
储存注意事项[13] 储存于阴凉、通风的不燃气体专用库房。远离火种、热源。库温不宜超过30℃。储区应备有泄漏应急处理设备。
合成方法
1.空分法 采用全低压流程,首先清除空气中灰尘和机械杂质,然后在压缩机中压缩,清除压缩空气中二氧化碳,干燥压缩空气,经液化、精馏,分离成氧和氮气。氮气贮藏在氮气柜;液氮送入贮槽,压缩的氮气充填氮气瓶中。
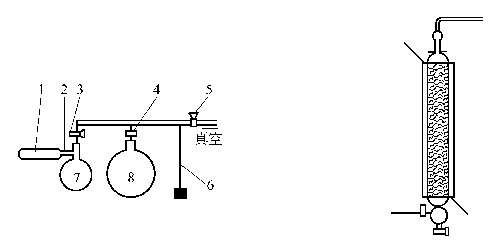
图XV-1 NaN3分解装置 利用活性铜提纯氮气装置
2.在如图所示的装置中,向长为40cm,直径为2cm的玻璃制分解管中装填数毫米厚,经重结晶并干燥的NaN3。磨口接头用湿布包裹使之冷却。用高真空泵将整个装置抽成真空,在保持真空下进行加热干燥。但装有NaN3的那根玻璃管不能加热到NaN3分解的温度。用高频真空检漏器检测系统是否漏气。这样做之后,用火焰均匀地加热管1。关闭活塞3,从一头依序将NaN3加热至开始分解。加热一段时间后停止加热,关闭活塞4和5,打开活塞3后,当确定压力计6的压力在增加,说明气体还在继续生成,当压力增加缓慢时,应再加热。如此继续操作直到在压力计上可以看到烧瓶中有了一些压力,制取了足够量的气体为止。当钠的细尘在烧瓶7中落下后,就可让气体进入烧瓶8。不要用玻璃棉来挡住钠的细尘。此操作不会有爆炸的危险,因为即使压力突然增加,最坏的结果也只不过是在2处将磨口冲开而已。此法制得的氮气已经很纯,无需再加纯制。NaN3的分解温度为280℃,KN3为360℃。
3.由钢瓶氮气纯制:钢瓶氮气中的水蒸气和CO2等杂质可用通常的洗涤剂除去,但除去痕量的氧气很困难。如需要高纯度的氮气最好选用下述的方法:装置如图,将长度为10m,电阻为64Ω的电热线直接缠绕在一根长75cm,直径4cm的玻璃管上。利用调压变压器将管子内的温度调节到约170℃。内管的外面再套上一个玻璃管以减少热量损失,同时试验时也可以观察内管中的现象。在内管中密封填充物,然后从内管的上面通入氢气,确认其中的空气被驱净后,即可通电加热。把还原CuO所生成的水从活塞中放走。当填充物全部变成暗紫色后,即可停止氢气,通入待纯制的氮气,填充物可用下列方法制得:
将120g Cu(OH)2CuCO3溶于2L浓氨水中,加入用盐酸洗过并经灼烧过的硅藻土420g,在水浴上蒸干。将其粉碎成3~5mm大小,在150~180℃彻底干燥至颗粒呈现棕色光泽。筛去细粉,得到产品。
图NaN3分解装置利用活性铜提纯氮气装置
1—加热管;2—磨口活塞;3,4,5—活塞;6—压力计;7,8—烧瓶2将250g CuCl2·H2O(或366g CuSO4·5H2O)溶于2L水中。加入用盐酸煮过并经过灼烧的硅藻土250g,加热至60℃,并在猛力搅拌下,将200g NaOH溶于500mL水的60℃溶液加入,10min后,将它倾入10L蒸馏水中。放置沉降,倾去上层清液,用蒸馏水用倾析法反复洗涤多次后抽吸过滤。将滤饼在螺旋手压机中压成3~5mm的细条,晾至半干后切成5~10mm细段,在180℃下烘干至恒重。
高纯氮一般以空气分离装置生产的氮气作为原料,通过化学法、吸附干燥法、变压吸附法及膜分离法等净化制成。
用途
1.用于合成氨、硝酸、氰氨化钙、氰化物、过氧化氢等生产。纯氮气用作防止氧化、挥发、易燃物质的保护气体、灯泡填充气。液氮主要用作冷源,用于仪器或机件的深度冷冻处理及食品速冻。也用于低温微粉碎用及电子工业等。
2.主要在集成电路、半导体和电真空器件、彩色显像管制造中用作保护气和运载气,化学气相淀积时的载气,液体扩散源的携带气,高温扩散炉中器件的保护气,还可用于石油、化工和氮分子激光器的生产中,且可作分析仪器载气,如标准气、校正气、平衡气及在线仪表标准气等。
3.纯氮用于化工、冶炼及电子工业,用作置换气、保护气。高纯氮用于标准混合气制备及电子工业中用作保护气、置换气、运载气及反应气。
4.用于合成氨,制硝酸,用作物质保护剂、冷冻剂等。[14]
安全信息
危险运输编码:UN1066 2.2
危险品标志:暂无
安全标识:S38
危险标识:暂无
文献
[1~14]参考书:危险化学品安全技术全书.第一卷/张海峰主编.—2版.北京;化学工业出版社,2007.6 ISBN 978-7-122-00165-8
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号