| 物竞编号 | 05Q4 |
|---|---|
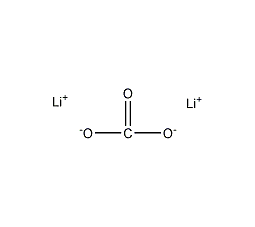
| 分子式 | Li2CO3 |
| 分子量 | 73.89 |
| 标签 | 高纯碳酸锂, 酸锂, Carbolith, Carbolithium, Lithonate, Candamide, Camcolit, 催化剂, 制药, 锂盐制备, 磁性材料原料及中间体 |
编号系统
CAS号:554-13-2
MDL号:MFCD00011084
EINECS号:209-062-5
RTECS号:OJ5800000
BRN号:3999191
PubChem号:24882220
物性数据
1. 性状:白色粉末状物质。
2. 密度(g/mL,25/4℃):2.11
3. 相对蒸汽密度(g/mL,空气=1):2.51
4. 熔点(ºC):720
5. 沸点:1310
6. 溶解性:不溶于醇和丙酮,溶于酸。微溶于水。
毒理学数据
1.具有明显的刺激作用,首先对胃肠道、肾脏和中枢神经系统有损害。
2.空气中最高允许浓度: 冷凝: 0.05mg/m3; 碎裂气溶胶:0.5mg/m3
生态学数据
其它有害作用:该物质对环境可能有危害,对水体应给予特别注意。
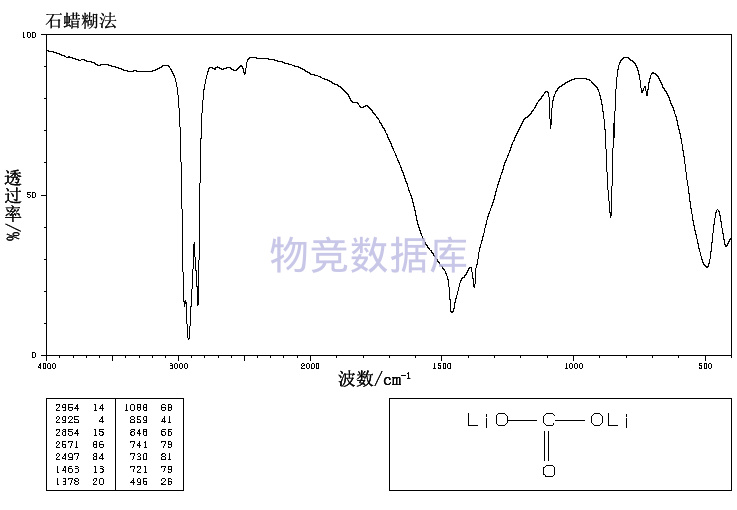
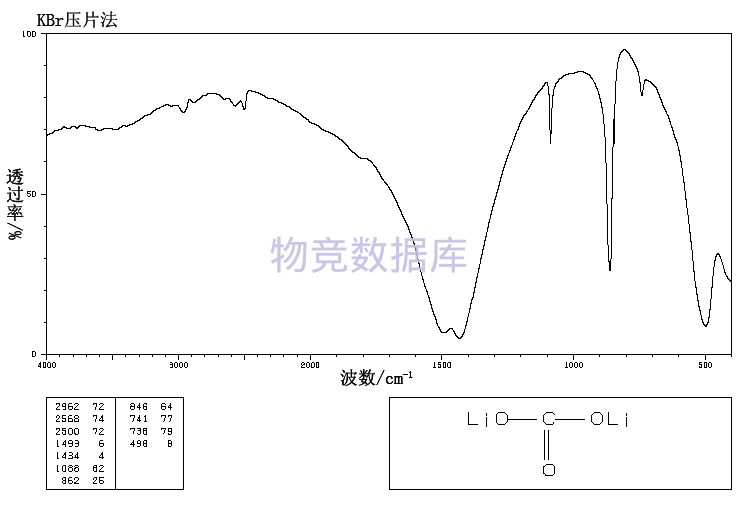
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:3
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积63.2
7.重原子数量:6
8.表面电荷:0
9.复杂度:18.8
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:3
性质与稳定性
1.不溶于醇,溶于酸。600 ℃以下对热稳定,618 ℃开始部分分解成氧化锂和二氧化碳。
贮存方法
1.贮存于通风干燥处,注意防雨淋水浸。
2.三合一复合袋内衬塑料袋包装,25kg/袋;或者纤维板桶包装,25kg/桶。密闭贮藏于阴凉、干燥、通风处。
3.不可与酸类物品接触.
合成方法
1.卤水综合利用法卤水经提取氯化钡后的含锂料液加入纯碱以除去料液内钙、镁离子,加入盐酸酸化,蒸发去除氯化钠,再经除铁,然后加入过量纯碱使碳酸锂沉淀,经水洗、离心分离、干燥,制得碳酸锂成品。其反应式如下:
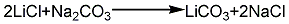
2.石灰烧结法锂辉石精矿(一般含氧化锂6%)和石灰石按1∶(2.5~3)重量比配料。混合磨细,在1150~1250 ℃下烧结生成铝酸锂和硅酸钙,经湿磨粉碎,用洗液浸出氢氧化锂,经沉降过滤,滤渣返回或洗涤除渣,浸出液经蒸发浓缩,然后加入碳酸钠生成碳酸锂,再经离心分离、干燥,制得碳酸锂成品。其反应式如下:
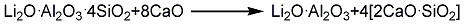
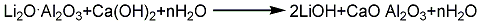
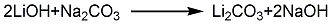
3.用氢氧化锂和二氧化碳为原料反应便可制得高纯度的碳酸锂,也可以用硫酸锂和碳酸钠为反应物,但碳酸锂易溶于其他盐溶液中,故产率不太高,一般为75%左右,而且产物中还会含有少量的硫酸锂。
精制法[13]称取25g碳酸锂,在室温下搅拌溶于2L水中,过滤除去不溶物质,激烈搅拌防止碳酸锂粘在烧杯壁上,慢慢加热至接近沸点,至完全沉淀,趁热过滤,再用沸水洗涤碳酸锂2~3次,在110℃下干燥,将滤液冷却,加入碳酸锂直至饱和,重复以上操作,可制得与第一次纯度基本相同的产物。
4.硫酸法 将熔融的锂辉石与硫酸反应,经净化后再与碳酸钠反应制得。石灰法 将焙烧的锂辉石与石灰乳反应,经净化后再与碳酸钠反应制得。副产法 由井盐卤制氯化钡后含锂的母液中提取。
5.以工业氢氧化锂为原料,加热水将其溶解后,滤去不溶物,趁热向滤液中通入干净二氧化碳气体至不再生成沉淀为止:
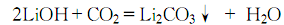
趁热过滤,甩干,用热蒸馏水洗涤至合格,于110℃烘干即可。将工业碳酸锂溶于冷水中,过滤后,滤液煮沸,停止加热,趁热过滤,热水洗涤、甩干、干燥,也能制得试剂碳酸锂。
用途
1.用于治疗狂燥性精神病,制作镇静剂等。是制取锂化合物和金属锂的原料。可作铝冶炼的电解浴添加剂。在玻璃、陶瓷、医药和食品等工业中应用广泛,亦可用于合成橡胶、染料、半导体及军事国防工业等方面。
2.用作抗躁狂药。用作搪瓷玻璃的添加剂,可增加搪瓷的光滑度,降低熔化点,并增强瓷器的耐酸、耐冷激、热激性能。在显像管制造中,它可提高显像管的稳定性并增加强度、清晰度,并降低表面粗糙度。还用于制造其他锂化合物、荧光粉及电解铝工业等。
3.用作光谱分析试剂,催化剂。用于锂盐制备,制药及陶瓷、玻璃工业。
4.用作铝冶炼的电解添加剂和用于电镀处理中。
安全信息
危险运输编码:UN 3264 8/PG 3
危险品标志: 有害
有害
安全标识:S8 S26 S43 S45 S24/25 S36/S37 S37/S39
危险标识:R22 R36 R41 R36/37/38 R36/38
文献
暂无
备注
暂无



 沪公网安备 31010602001115号
沪公网安备 31010602001115号