| 物竞编号 | 0869 |
|---|---|
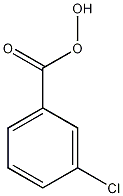
| 分子式 | C7H5ClO3 |
| 分子量 | 172.57 |
| 标签 | 间氯过氧苯甲酸, 3-Chloroperbenzoic acid, 脂肪族羧酸及其衍生物 |
编号系统
CAS号:937-14-4
MDL号:MFCD00002127
EINECS号:213-322-3
RTECS号:SD9470000
BRN号:608317
PubChem号:24855622
物性数据
1. 性状:白色结晶
2. 密度(g/mL,25/4℃):0.56
3. 相对蒸汽密度(g/mL,空气=1):未确定
4. 熔点(ºC):92-94℃(分解)
5. 沸点(ºC,常压):未确定
6. 沸点(ºC,5.2kPa):未确定
7. 折射率:未确定
8. 闪点(ºC):未确定
9. 比旋光度(º):未确定
10. 自燃点或引燃温度(ºC):未确定
11. 蒸气压(kPa,25ºC):未确定
12. 饱和蒸气压(kPa,60ºC):未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:几乎不溶于水,易溶于乙醇、醚类,溶于氯仿、二氯乙烷。
毒理学数据
暂无
生态学数据
对水是稍微有害的,不要让未稀释或大量的产品接触地下水,水道或者污水系统,若无政府许可,勿将材料排入周围环境。
分子结构数据
1、 摩尔折射率:39.82
2、 摩尔体积(cm3/mol):120.2
3、 等张比容(90.2K):324.9
4、 表面张力(dyne/cm):53.2
5、 极化率(10-24cm3):15.78
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:1
3.氢键受体数量:3
4.可旋转化学键数量:2
5.互变异构体数量:无
6.拓扑分子极性表面积46.5
7.重原子数量:11
8.表面电荷:0
9.复杂度:149
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.常温常压下稳定,避免氧化物 有机材料 还原剂 碱 热 金属粉末接触。
2.本品对皮肤有刺激作用,能引起发炎。应穿戴防护手套、防护衣、防护眼镜。
3.对撞击敏感,能迅速燃烧,有爆炸危险,反应时要小心处理。存储在盛有聚乙烯的容器中,并保存在冰箱中。
贮存方法
1.保持容器密封,储存在阴凉,干燥的地方。
2.本品常温、常压下稳定。贮存时远离易燃性物料。避免受热、火花、灼烧、碰撞摩擦。
合成方法
1.在聚乙烯容器中,加入1.5g七水硫酸镁、36g氢氧化钠、360ml水、90ml30%双氧水、450ml二氧六环和冰块,使温度降至15℃,在激烈搅拌下,加入52.5g间氯苯甲酰氯,再加入冰块,维持温度在25℃以下。反应15min后,加入900ml20%冷硫酸。静置,分出有机层,过滤,滤液蒸出溶剂(高真空蒸馏),得51g 3-氯过苯甲酸。
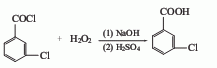
2.制法:
于1L的烧杯中,加入七水硫酸镁0.3g,水75mL,氢氧化钠7.2g,溶解后冷却至室温,加入30%的H2O218mL和二氧六环90mL。冰水浴冷却至15℃以下,剧烈搅拌下一次加入间氯苯甲酰氯(2)10.5g(0.06mol),保持反应温度不超过25℃,必要时可加入适量的碎冰。搅拌反应15min。用20%的稀硫酸调至酸性。以二氯甲烷提取四次。合并二氯甲烷层,水洗,减压蒸出溶剂至干,得白色片状结晶间氯过氧苯甲酸(1),以碘量法测定,含约80%的活泼氧。[1]
用途
1.本品中含间氯苯甲酸过氧化物为80%-85%,其余为间氯苯甲酸。它广泛用于环化反应、Baeyer-Villiger反应、N-氧化反应和S-氧化反应等。它可用作合成医药、农药等精细化工产品的氧化剂使用;另外,有时也用作漂白剂。可用作氧化剂,漂白剂等。
2.间氯过苯甲酸是一种良好的亲电试剂,能和许多官能团发生反应,可以氧化烯烃、烯醇硅醚、呋喃、硫化物、硒化物和氨基化合物等[1]。
官能团的氧化 m-CPBA中弱的O-O键可以与多电子的底物反应将氧原子转移到底物上。酮和醛会发生氧的插入反应(Baeyer- Villiger氧化反应)。有机过酸容易与烯烃发生环氧化反应,此反应为顺式立体专一性反应。对酸敏感的环氧化物在合成时pH必须使用NaHCO3或m-CPBA-KF试剂来控制[2]。
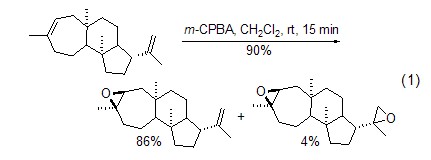
区域选择性环氧化 单烯烃环加成反应中,由于烷基的供电子效应,反应速率为:四取代和三取代烯烃>二取代烯烃>单取代烯烃。在有双键的二烯烃的环加成反应中可以观察到高的区域选择性 (式1)[3]。
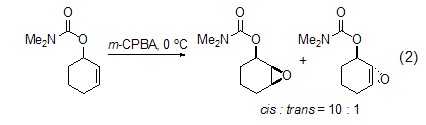
环烯烃的非对映选择环氧化 烯丙醚的环氧化反应中因为烯丙基取代阻碍了从α面接近反应物的途径,当体积巨大的O-t-Bu基团加在烯丙基碳上时有很高的立体选择性;而无位阻的亚甲基环己烷及类似化合物的环氧化优先发生在直立键方向。烯丙基氨基甲酸酯环氧化的主产物是顺式结构 (式2)[4]。
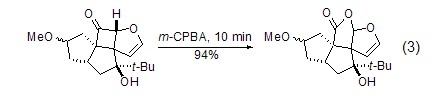
Baeyer-Villiger重排 酮与过酸反应可生成酯。环酮与H2O2在碱性条件下发生Baeyer- Villiger重排生成γ-内酯 (式3)[5]。
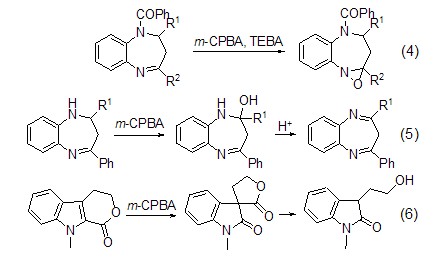
含氮化合物的氧化 一级胺被m-CPBA氧化成相应的硝基化合物,而二级胺氧化成羟胺并产生副产物硝酮。N-杂环的m-CPBA氧化反应生成对应的N-氧化物,如m-CPBA与异唑反应生成硝酮,而(–)-异唑则生成(–)-环戊酮。m-CPBA也可使N,N-二甲基腙裂分为酮。对于碳氮双键,不存在氨基时由m-CPBA氧化可以得到三元环,但同时存在氨基则在氧化得到醇后经重排可以形成碳氮双键 (式4,式5)[6]。N-取代吲哚δ-内酯在Kurihara条件下得不到预期的酮酰胺,却形成了新的杂环化合物 (式6)[7]。
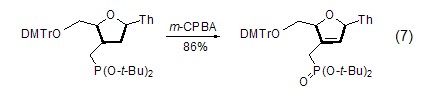
含磷、硫、硒、碘化合物的氧化 m-CPBA氧化亚磷酸酯可立体专一性地生成磷酸盐 (式7)[8]。硫化物在m-CPBA作用下被选择性的氧化成亚砜。
安全信息
危险运输编码:UN 3106 5.2
危险品标志: 氧化剂
氧化剂  腐蚀
腐蚀
安全标识:S14 S26 S45 S36/S37/S39
文献
[1]参考文献:1、Richard N M,Richard N S,James E D.Org Synth,1988,Coll Vol 6:276.2、Robert M H,Kenneth R W.J Org Chem,1957,22:1142. 参考书:有机化合物合成手册/孙昌俊,王秀菊,孙风云主编. 北京:化学工业出版社,2011.8 ISBN 978-122-11519-5
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号