主族金属有机超分子化学进展
- 2012-06-11
- 专题
超分子化学是研究分子间弱相互作用和分子组装的化学。它是现代化学和材料科学中最有活力的研究领域之一[1],尤其在可逆相催化[2],主客体分子或离子交换[3~5],和形形色色的光电磁分子器件[6~8]等方面已显示了诱人的应用前景。学者在这一领域的研究相当活跃[1~19]。有机金属化学是较为成熟的化学分支[20, 21],而有机主族金属化合物由于其本身丰富的化学和广泛的应用前景正越来越受到关注[22~30],如不少有机主族金属化合物是很好的MOCVD前驱体[22~25]。因此将形形色色的有机主族金属化合物作为基本单元,通过自组装形成更复杂的超分子排列,正在成为超分子化学和有机金属化学的共同研究热点[9]。许多有机主族金属化合物不仅具有自组装能力,形成结构各异的超分子化合物,而且某些物理化学性质因此得到了修饰或加强,使其应用前景更为广阔。例如,法国Bruno Chaudret等人研究发现以金属有机超分子[CpIn]为前躯体可进行In 纳米粒子多维空间结构的自组装[31]以及In-Sn纳米导线的合成[32]。
有机主族金属化合物通过弱的分子间作用力组装形成超分子时,主要的成键方式是:“Dative键”(配位键)、“Secondary”键(次级键)、氢键和p键作用[9]。配位键弱于共价键,强于次级键。如第三主族的Al(Ⅲ)、Ga(Ⅲ)、In(Ⅲ)、Tl (Ⅲ)的有机金属化合物常以配位键形成环状或笼状超分子化合物,而低价态的In(Ⅰ)、Tl(Ⅰ)则常以更弱的次级键形成超分子化合物。次级键可表示为X A…Y,弱于配位键,与氢键相当。位于元素周期表底部的主族p区重金属化合物与一些软酸软碱相互作用时易形成次级键。次级键虽然较弱,但在主族p区重金属元素形成超分子的过程中却非常重要。限于篇幅,我们只讨论含6种常见的p区重金属In、Tl、Sn、Pb、Sb和Bi的若干典型有机主族金属超分子的自组装和结构。
1 含铟、铊有机金属化合物的自组装
ⅢA 族元素铝、镓、铟的有机金属化合物在许多领域具有重要的应用价值。例如,可在半导体材料方面用作材料生长的前驱体[33],还可用作高效率、高亮度的有机电致发光材料等[34, 35]。ⅢA族的三价金属有机化合物是三配位的缺电子体系(Lewis 酸),有较强的自组装能力,随着原子半径的增大及金属性的增强,有机铟、铊化合物的配位数相应增加,常常以次级键组装形成超分子。较常见的有链状和梯状超分子,如化合物[Me2In(CN)]∞[36](图1)是由氰根架桥形成的一维螺旋链状结构。其中,In(Ⅲ)是四配位的,与2个甲基、1个氰根以M C共价键相连,与另一结构单元中的氰根形成M←N 配位键(键长为2.260)。有机In(Ⅲ)化合物还常通过金属与卤素间的弱相互作用(次级键等)形成超分子构型。如MeInCl2[37]和RInCl2[38](R = tBuCH2),这2个化合物中In(Ⅲ)均为五配位,但由于有机基团空间位阻的影响,它们的空间构型却不尽相同。如图2所示,MeInCl2单元中有1个Cl和相邻2个In以次级键(键长a=3.203和b=3.799)相连形成一维梯状结构。在RInCl2 (R=tBuCH2)中(图3),2个Cl均以次级键(键长2.700~2.821)连接相邻的In而成一维链状结构。
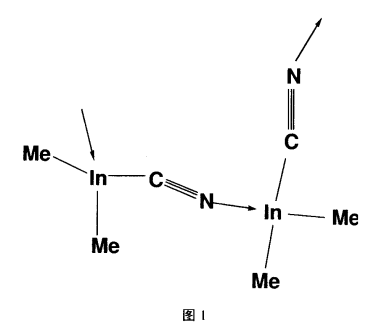
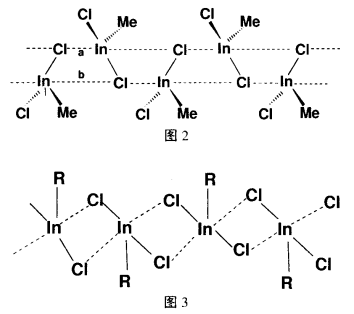
铊化合物的自组装形式多样,结构丰富。Tl(Ⅲ)对氧的亲合力较强,常通过配位键组装形成超分子,尤其可以使铊与一些较难配位的配体(如高氯酸根和mesylamide 等)配位形成形状各异的超分子化合物。如R2TlN(SO2Me)2[39](R=Me3SiCH2)(图4),R2Tl 与[N(SO2Me)2]-配体中的氮原子以共价键相连,同时又和相邻配体中的氧原子以次级键(Tl…O=2.799 和2.813)连接成1个二维网状结构。
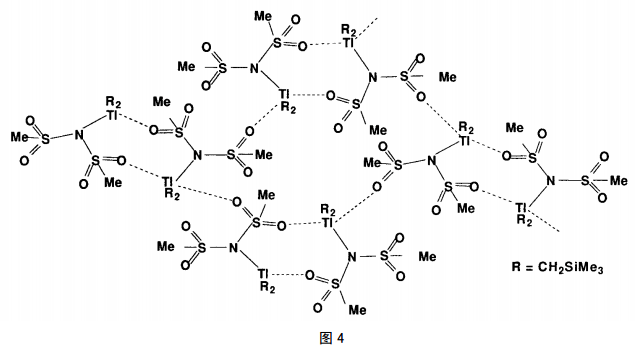
此外,以Tl…S次级键自组装形成的超分子体系在Tl (Ⅲ)化合物中也是很常见的(Ph2PS2TlCy2)2[40]就是其中一例。如图5所示,在每一结构单元内,Tl(Ⅲ)是六配位的,每个Tl原子与配体分子中的2个硫原子以共价键配位(a=2.789,b=2.816);同时,与相邻结构单元中的2个S形成次级键(c=3.563,d=3.616) ,形成双桥梯状超分子排列。
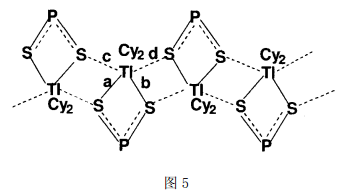
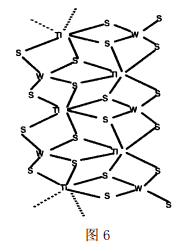
Tl(Ⅰ)也易于形成超分子化合物,且其超分子化合物也表现出良好的物理化学特性。 例如,我们曾通过低加热固相法和微波辐照法合成了Tl(Ⅰ)化合物[(n-Bu)4N][TlMS4] (M=Mo,W)[41, 42]。它是由四硫代钼酸盐或四硫代钨酸盐和铊(Ⅰ)形成的一维链状聚合物(图6),其中Tl(Ⅰ)以配位键和S相结合(Tl←S = 3.007、3.387),这2个化合物在DMF溶液中还表现出较好的三次非线性光学性质[42]。
另一个例子是[(Cp*WS3Tl)2]n[43]。它是由[(Cp*WS3)2Tl4]单元通过2个Cp*WS3桥联形成的一维链状聚合物(图7)。其中,Tl-S配位键键长约为2.890(6)~3.070(7), Tl…S 次级键键长为3.506(4) 和3.432。
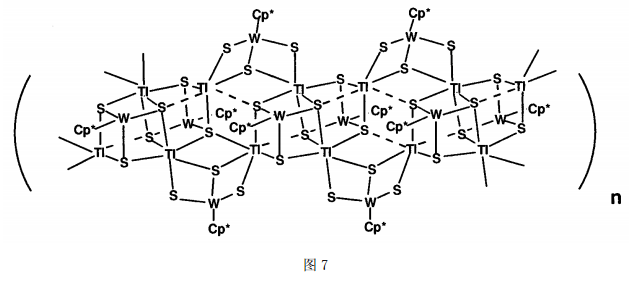
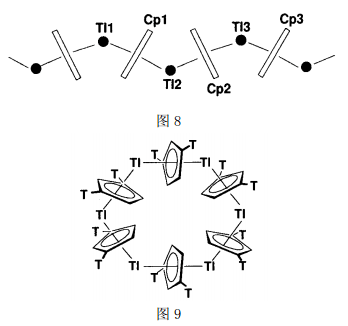
有机铊(Ⅰ)还可通过p-键作用形成超分子化合物,这在IIIA族中是很少见的。[CpTl]就是很好的例子,它不仅是合成其它茂基化合物的前驱体[44],而且它们的分子结构也十分有特色。图8 是较典型的[CpTl][45]的超分子组装构型,以[CpTl]为基本单元,相邻Tl(Ⅰ)之间以Cp连接而成的一维Zigzag链。已有报道的Tl(Ⅰ)与Cp衍生物的超分子组装类型还有较为特殊的[Cp2TTl]6 (Cp2T=1,3-(SiMe3)2Cp)[46]图9),其中Cp2T作为桥基将金属Tl连接成环,Tl处于六边形的角顶,并以近似于sp2杂化的σ轨道成键而形成六边形结构。
2 含锡、铅有机金属化合物的自组装
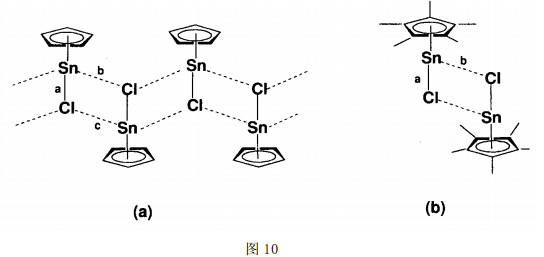
近年来,由于有些有机锡化合物是有机反应的良好Lewis酸催化剂,还有些具有抗癌活性,因而此类化合物受到广泛的关注[47, 48]。 有意思的是,不少有机锡化合物易形成超分子结构。例如,[CpSnCl]n[49]的超分子构型是一维带状结构(图10a),不对称的Sn…Cl桥将CpSnCl单元联结。其中,Sn-Cl共价键键长为a=2.679,而Sn…Cl次级键键长则为b=3.242和c=3.262。[Cp*SnCl]2[50]分子中也存在次级键,但可能因为五甲基环戊二烯基较大的空间位阻形成了二聚体(图10b)。
单烷基Sn 化合物与氧易形成种类繁多的SnO簇状超分子[51]。这些簇合物具有合成简单,稳定性好,易溶解等优点。含{(RSn)12(μ3- O)14(μ2-OH)6}2+大阳离子的簇合物(图11中的结构单元, R=饱和碳链-(CH2)n-, n=3~5,8)是合成锡氧无机有机混合材料的良好的纳米基本单元。由于SnCsp3键的稳定性,即使遇到水也不易分解,所以{(RSn)12(μ3-O)14(μ2-OH)6}Cl2还可以通过有机网络装配起来(如图11, 各单元间的连线就表示饱和碳链-(CH2)n-)。

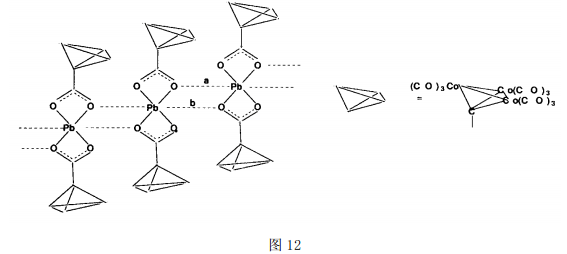
由于有机铅的毒性,对其超分子化合物的研究相对较少。但即使如此,仍有不少新型化合物被报道。例如[Pb{(CO)9Co3(μ-CCOO)}2][52]就有着特殊的超分子结构(如图12): Pb(μ-O)2Pb链插入羰基钴簇合物单元之间,而羰基则暴露于外界;结构单元间以Pb…O 次级键相连,键长为2.717(a) 和2.837(b)。研究还表明,该物质的高温分解产物在2-丁烯的加氢反应中有催化活性[52]。
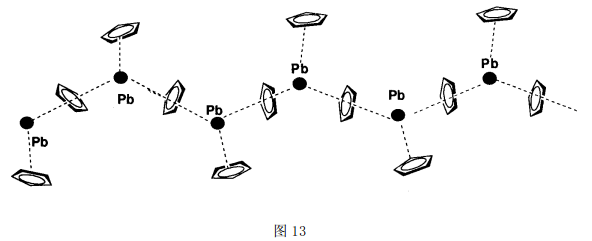
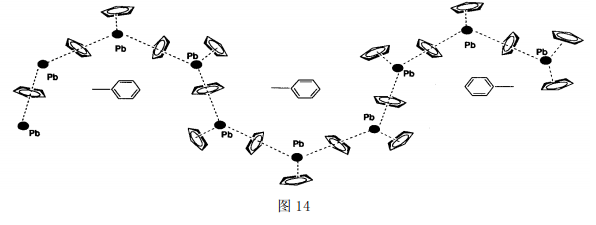
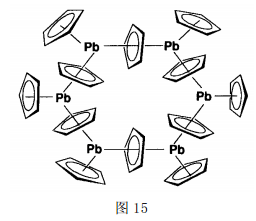
锡、铅与环戊二烯基及其衍生物的化合物也具有较强的自组装能力,且分子结构很有特色。以Pb(Ⅱ)为例,最初的[PbCp2]单晶是通过真空升华获得的,X-射线衍射表明,其结构为一维Zigzag链[53](图13),[PbCp2]结构单元通过Cp桥联,端基Cp与Pb间的键长约为2.511~2.615而桥联Cp与Pb 间次级键的键长约为2.728~2.911。该化合物还可通过丙酮和四氢呋喃混合溶剂结晶制得。近年来的研究表明,[PbCp2]至少还有其它2种不同的超分子结构[54]。一种是聚合的甲苯溶剂化物(图14),该聚合物链不是简单的一维Zigzag链状结构,而是采用了类似正弦曲线的结构,以避开插入的甲苯分子。 另一种是6个相同的[PbCp2]结构单元结合成的环状结构,而这些[PbCp2]6 环又通过晶格堆积成了无限圆柱状孔道(图15)。
此外,我们最近以PbCl2与[PPh4][Cp*WS3]在DMF 中反应得到了1 个新颖的聚合物[Cp*WS3PbCl]n[43],它是由[(Cp*WS3)2Pb2]簇单元通过4个线性Pb-Cl-Pb 桥联而成的二维网状结构(图16),其中Pb-Cl键长为2.7911(2),而Pb-S键长为2.886(1)~2.913(1),比簇合物[Mo3S4(PbI3) (dtp)3(C3H4N2)3][(CH3)2CO]2 的Pb-S键长(约3.027)稍短[55,56]。

3 含锑、铋有机金属化合物的自组装
有机锑超分子化合物的例子很多,如[Me3Sb- Cl2·SbCl3][57], [Ph3SbCl2·SbCl3][58]
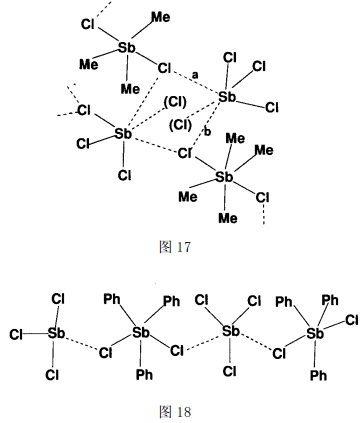
和 [(C4H8)(Me)- SbCl2] [59]。在[Me3SbCl2·SbCl3] 中,Me3SbCl2和SbCl3成对地通过Sb…Cl次级键 (a=3.203)相连成一维链,链与链之间再以Sb…Cl (b=3.308)形成双链结构(图17)。在[Ph3SbCl2·SbCl3]中是Ph3SbCl2和SbCl3成键的主要特征在于:Ph3SbCl2分子中的2个Cl原子分别与相邻的SbCl3中的Sb原子形成弱的次级键形成四核链状化合物(Sb…Cl次级键键长为3.236和3.287)(图18)。
在[(C4H8)(Me)SbCl2]中,4个(C4H8)(Me)SbCl2通过Sb…Cl次级键(3.613)相互联结成超分子“框”(图19)。
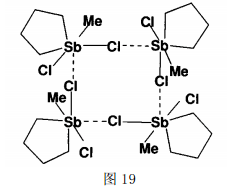
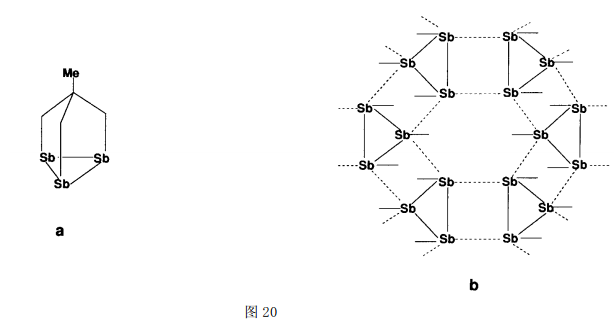
以Sb…Sb 次级键形成的有机锑(Ⅲ)化合物也有报道。例如,固态的MeC(CH2)3Sb3是1个漂亮的二维笼状结构[60]。其中的基本单元如图20a,6个这样的单元通过Sb…Sb次级键(3.97和4.01)联结成类六边形结构,这个结构再和邻近的基本单元相连成二维结构。
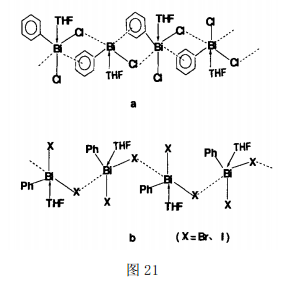
在有机主族金属超分子化学中,有机铋(Ⅲ)化合物也扮演了一定的角色[27]。如图21 所示,[PhBiCl2·THF]和[PhBiX2·THF] (X=Br、I) [61]均为一维聚合物链。不同的是,前者不仅以Cl为桥,苯基也通过弱的π键作用将相邻的Bi原子相连,其一维链的结构单元[Bi(μ-Cl)(μ-Ph)Bi];后者则只有卤素与Bi原子以次级键相连。
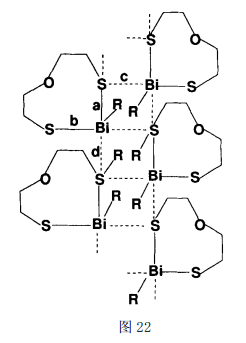
又如,RBi(SCH2CH2OCH2CH2S) (R=Ph) 中Bi 与硫原子以次级键形成的双链聚合物结构(图22),在这个结构中, Bi�S共价键(a=2.560, b=2.562)和Bi…S次级键(c=3.440, d=3.590)存在着明显的差别[62]。
我们通过控制[PPh4][Cp*WS3]/BiCl3/PPh4Cl的摩尔比(1:2:1或1:3:1)分别得到2个杂核簇合物: [PPh4]2[Cp*WS3(BiCl3)2Cl] 和[PPh4]2[Cp*WS3- (BiCl3)3Cl][63, 64]。前者如图23a所示,1个Cp*WS3和2个BiCl3通过μ2- 和μ3-S桥相连形成蝴蝶形结构,额外的第7个Cl–再以次级键(Bi…Cl=2.872)和2个Bi(III)联结形成1个缺口立方烷结构。 后者如图23b所示,1个Cp*WS3单元和3个BiCl3形成缺口立方烷结构,而额外的第10个Cl–和3个Bi(Ⅲ)以类似的次级键(Bi…Cl=2.998)形成1个闭合的类立方烷结构。预期控制[PPh4][Cp*MS3] (M = Mo, W) 和主族金属 (如In, Sn, Pb, Sb, Bi, Tl)的摩尔比,可以获得更多有意思的主副族含簇超分子化合物,并且此类化合物可能有较好的三次非线性光学性质,例如 [PPh4]2[Cp*WS3 (BiCl3)3Cl]的三次非线性极化率χ(3)=7.558×10-14esu,响应时间为28 ps。这方面的研究正在进行中。
4 结束语
综上所述,超分子的自组装在有机主族金属化合物中是比较普遍的。许多有机主族金属超分子化合物的成键方式及结构独特,并表现出潜在的应用前景,值得进一步深入研究和探讨。 此外,除了上述的有机主族金属超分子外,对于其它有机金属超分子化学的研究(有机过渡金属,有机稀土金属等)近年来也取得了很大的进展[9]。因此,对有机金属超分子化学的研究,将不仅仅是超分子化学和有机金属化学的一种简单结合,更有助于超分子化学和有机金属化学的共同发展。

参 考 文 献
(1) Lehn, J. M.; Atwood, J. L.; Davis, J. E. D.; MacNicol, D. D.; Vogtle, F. Comprehensive Supramolecular Chemistry, Pergamon Press: Oxford, U. K. 1996, Vols. 1�11.
(2) Ito, H.; Kusukawa, T.; Fujita, M. Chem. Lett. 2000, 6, 598 599.
(3) Hong, M. C.; Zhao, Y.; Su, W.; Cao, R.; Fujita, M.; Zhou, Z.; Chan, A. S. C. Angew. Chem. Int. Ed. Engl. 2000, 39, 246 2470.
(4) Slone, R. V.; Benkstein, K. D.; Belanger, S.; Hupp, J. T.; Guzei, I. A.; Rheingold, A. L. Coord. Chem. Res. 1998, 171, 221 243.
(5) Beer, P. D.; Szemes, F.; Balzani, V.; Sala, C. M.; Drew, M. G. B.; Dent, S. W.; Maestri, M. J. Am. Chem. Soc. 1997, 119, 11864 11875.
(6) Lent, C. S. Science 2000, 288, 1597 1599.
(7) Breuning, E.; Ruben, M.; Lehn, J. M.; Renz, F.; Garcia, Y.; Ksenofontov, V.; Gutlich, P.; Wegelius, E.; Rissanen, K. Angew. Chem. Int. Ed. Engl. 2000, 39, 2504 2507.
(8) Holliday, B. J.; Mirkin, C. A. Angew. Chem. Int. Ed. Engl. 2001, 40, 2022 2043.
(9) Haidue, I.; Edelmann, F. T. Supramolecular Organometallic Chemistry. WILEY-VCH, Weinheim, <st1:country-region w:st="on">Germany 1999.
(10) Kang, J.; Santamaria, J.; Hilmersson, G.; Rebek, J. J. Am. Chem. Soc. 1998, 120, 7389 7390.
(11) Cotton, F. A.; Daniels, L. M.; Lin, C.; Murillo, C. A. Chem. Commun.1999, 841 842.
(12) Hong, M. C.; Zhao, Y. J.; Su, W. P.; Cao, R.; Fujita, M.; Zhou, Z. Y.; Chan, A. S. C. J. Am. Chem. Soc. 2000, 122, 4819 4820 .
(13) Xiong, R. G.; You, X. Z.; Abrahams, B. F.; Xue, Z. L.; Che, C. M. Angew. Chem. Int. Ed. Engl. 2001, 40, 4422 4425.
(14) Ma, B. Q.; Gao, S.; Su, G.; Xu, G. X. Angew. Chem. Int. Ed. Engl. 2001, 40, 434 437.
(15) Fang, C. J.; Duan, C. Y.; He, C.; Meng, Q. J. Chem. Commun. 2000, 1187 1188.
(16) Zheng, S. L.; Tong, M. L.; Fu, R. W.; Chen, X. M.; Ni, S. G. Inorg. Chem. 2001, 40, 3562 3569.
(17) Liu, H. K.; Sun, W. Y.; Ma, D. J.; Yu, K. B.; Tang, W. X. Chem. Commun. 2001, 591 592.
(18) Zhang, L.; Cheng, P.; Tang, L. F.; Weng, L. H.; Jiang, Z. H.; Liao, D. Z.; Yan, S. P.; Wang, G. L. Chem. Commun. 2000, 717 718.
(19) Feng, S. H.; Xu, R. R. Acc. Chem. Res. 2001, 34, 239 247.
(20) Abel, E. W.; Stone, F. G. A.; Wilkinson, G. Comprehensive Organometallic Chemistry Pergamon, New York 1995.
(21) 钱延龙, 陈新滋编著, 金属有机化学与催化. 化学工业出版社,北京1999.
(22) Manasevit, H. M. Appl. Phys. Lett. 1969, 116, 1725.
(23) 游效曾, 孟庆金, 韩万书编著, 配位化学进展. 高等教育出版社,北京2000, 121�131.
(24) Zhao, Q.; Sun, H. S.; You, X. Organometallics 1998, 17, 156 160.
(25) Sievers, R. E.; Turnipseed, S. B.; Huang, L. Coord. Chem. Rev. 1993, 128, 285.
(26) Kiss, T.; Sovago, I.; Toth, I.; Lakatos, A.; Bertani, R.; Tapparo, A.; Bombi, G.; Martin, R. B. J. Chem. Soc., Dalton Trans. 1997, 11, 1967 1972.
(27) Uchhiyama, Y.; Kano, N.; Kawashima, T. Organometallics 2001, 20, 2440 2442.
(28) Silvestru, C.; Breuning, H. J.; Althaus, H. Chem. Rev. 1999, 99, 3277 3327.
(29) Jagirdr, B. R.; Murphy, E. F.; Roesky, H. W. Prog. Inorg. Chem, 1999, 48, 351 455.
(30) Schmidt, M. W.; Finger, L. W.; Angel, R. J.; Dinnebier, R. E. Am. Mineral 1998, 83, 881 888.
(31) Soulantica, K.; Maisonnat, A.; Fromen, M. C.; Casanove, M. J.; Lecante, P.; Chaudret, B. Angew. Chem. Int. Ed. Engl. 2001, 40, 448 451.
(32) Soulantica, K.; Froment, A.; Senocq, F. Angew. Chem. Int. Ed. Engl. 2001, 40, 2984 2986.
(33) Jones, A. C. Chem. So. Rev. 1997, 26, 101 110.
(34) Tang, C. W.; Vanslyke, S. A. Appli. Phys. Lett. 1987, 51, 913 915.
(35) 吴雪松, 潘毅, 孙祥祯, 朱玉. 结构化学 1999, 18, 418 421.
(36) Blank, J.; Hausen, H. D.; Weidlein J. J. Organomet. Chem. 1993, 444, C4.
(37) Mertz, K.; Schwarz, W.; Zettler, F.; Hausen, H. D. Z. Naturforsch 1975, 30b, 159 161.
(38) Beachley, O. T. J.; Spiegel, E. F.; Kopasz, J. P.; Rogers, R. D. Organometallics 1989, 8, 1915 1921.
(39) Blaschette, A.; Jones, P. G.; Michalides, A.; Naveke, M. J. Organomet. Chem. 1991, 415, 25 37.
(40) Casas, J. S.; Castellano, E. E.; Castineiras, A.; Sanchez, A.; Sordo, J.; Vazquez-Lopez, E. M.; Zukerman-Schpector, J. J. Chem. Soc., Dalton Trans. 1995, 1403 1409.
(41) Lang, J. P.; Liu, J.; Chen, M. Q.; Lu, J. M.; Bian, G. Q.; Xin, X. Q. J. Chem. Soc., Chem. Commun. 1994, 2665 2666.
(42) Lang, J. P.; Tatsumi, K.; Kawaguchi, H.; Lu, J. M.; Ge, P.; Ji, W.; Shi, S. Inorg. Chem. 1996, 35, 7924 7927.
(43) Lang, J. P.; Tatsumi, K. Inorg. Chem. submitted.
(44) Cotton, F. A.; Wilkinson, G.; Murillo, C. A.; Bochmann, M. Advanced Inorganic Chemistry, JohnWiley & Sons, 6th Ed, New York 1999, 206.
(45) Blom, R.; Werner, H.; Wolf, J. J. Organomet. Chem. 1988, 354, 293 299.
(46) Harvey, S.; Raston, C. L.; Skelton, B. W.; White, A. H.; Lappert, M. F.; Srivastava, G. J. Organomet. Chem. 1987, 328, C1 4.
(47) Song, X. Q.; Yang, Z. Q.; Xie, Q. L. Chin. J. Struct. Chem. 1993, 18, 84 88.
(48) Qin, Y.; Wu, L.; Zhao, J.; Kang Y.; Tang, Y.; Yao, Y. Chem. Lett. 2000, 8, 950 951.
(49) Boss, K. D.; Buten, E. J.; Noltes, J. G.; Spek, A. L. J. Organomet. Chem. 1975, 99, 71 77.
(50) Constantine, S. P.; Lima, G. M. D.; Hitchcock, P. B.; Keats, J. M.; Lewless G. A.; Marziano, I. Organometallics 1997, 16, 793 795.
(51) Zobel, B.; Duthie, A.; Dakternieks, D.; Tiekink, E. R. T. Organometallics 2001, 20, 2820 2826.
(52) Lei, X. J.; Sheng, M. Y.; Patil, A.; Wolf, E. E.; Fehlneer, T. D. Inorg. Chem. 1996, 35, 3217 3222.
(53) Overby, J. S.; Hanusa, T. P.; Young, V. G. Inorg. Chem. 1998, 37, 163 165.
(54) Beswick, M. A.; Russell, C. A.; Steine, R. A.; Wright, D. S. J. Chem. Soc. Chem. Commun. 1997, 109 110.
(55) 卢绍芳; 黄健全; 黄小荥; 吴锵全; 余荣民. 化学学报 1998, 56, 905 913.
(56) Yu, R. M.; Lu, S. F.; Hang, X. Y.; Wu, Q. J.; Huang, J. Q. Inorg. Chem. 1999, 38, 3313 3315.
(57) Almenningen, A.; Gunderssen, G.; Marchetti, F.; Zannazzi, D. F. J. Chem. Soc. Chem. Commun. 1981, 181 182.
(58) Hall, M.; Sowerby, D. B. J. Chem. Soc., Dalton Trans. 1983, 1095 1099.
(59) Meinema, H. A.; Noltes, J. G.; Spek, A. L.; Duisenberg, A. J. M. Recl. Trav. Chim. Pays-Bas 1988, 107, 226 229.
(60) Ellermann, J.; Kock, E.; Burzlaff, H. Acta Cryst. 1985, C41, 1437 1439.
(61) Norman, N. C. Phosphorus, Sulfur, Silicon 1994, 87, 167 174.
(62) Drager, M.; Schmidt, B. M. J. Organomet. Chem. 1985, 290, 133 139.
(63) Lang, J. P.; Kawaguchi, H.; Tatsumi, K. The 74th Spring Meeting of Japan Chemical Society, Kyoto, Japan 1998, 517.
(64) Lang, J. P.; Tatsumi, K. The 78th Spring Meeting of Japan Chemical Society, Tokyo, Japan 2000, 467.
注:本文为提供者整理翻译的,由于知识所限,错误在所难免,敬请原谅。如有问题可以查找原文。



 沪公网安备 31010602001115号
沪公网安备 31010602001115号