微波技术在无机固相材料合成中的应用
- 2012-12-06
- 专题
开发合成固相材料的新方法是材料化学领域里的一个重要研究方向。这既是开发快速、节能的新型材料制备方法的需要,同时也是避免实验过程中的副反应及挑战采用热力学中的可逆过程来合成亚稳相的需要。近年来,微波辅助技术作为一种新型的合成方法[1~5],得到了迅速发展,为功能材料的制备提供了更为可靠的途径,显现出越来越大的重要性。与传统方法相比,微波合成技术具有更快速、更洁净以及更经济的优点。人们已经通过微波法合成了许多物质,包括碳化物、氮化物、复杂氧化物、硅化物、硅酸盐以及磷灰石等。这些材料无论是在工业生产还是科学研究方面都是很重要的。
微波是一种普遍存在的电磁波,其波长在1cm~1m之间,位于红外辐射和无线电波之间,相应频率为 0.3~300GHz。波长在1~25cm之间的微波常用于雷达发射,其余的微波则广泛应用于通讯行业。用于加热的微波波长一般为12.2cm(2.45GHz)或32.8cm(915MHz)。微波加热是电磁能以波的形式辐射到介质内部,利用介质的介电损耗发热。与常规加热相比,微波加热不需热的传导和对流,在极短时间内使介质分子达到活化状态,加剧分子的运动与碰撞,可大大加快反应速度,缩短反应周期,并因内外同时加热,体系受热均匀,无滞后效应。
Clark等[6]从多个方面综合阐述了微波技术的应用。利用微波技术合成材料,其速度更快、操作更简单,同时更能有效地利用能源。虽然在利用微波技术合成材料的过程中,微波与反应物间相互作用的实质还不是很清楚,但人们通常认为无论是在有快速加热引起的共振状态,还是松弛状态,能量从微波到材料之间的传递都是在不断进行的。目前,报道利用微波技术成功合成各类无机固相材料的文献很多。其中,一些新的观点引起了人们的广泛关注和讨论[7~9]。为了给科学研究提供必要的理论基础,下文首先将对微波与材料之间的相互作用加以说明。
1微波加热原理
一般来讲,根据材料与微波之间的相互作用,可以将材料分为三大类[10]:(1)微波反射材料,主要是块体金属与合金,例如黄铜等,可利用这类材料制成微波导航器;(2)微波透射材料,这类材料可以透射微波,主要是石英、锆石、部分玻璃和陶瓷、聚四氟乙烯等,这些材料对微波是透明的,几乎不吸收微波能,可用作烹饪或实验的用具和容器;(3)微波吸收材料,是一类最为重要的材料,它们能够有效地吸收微波的能量并得以迅速加热,因此可以利用微波加热的方式进行合成。
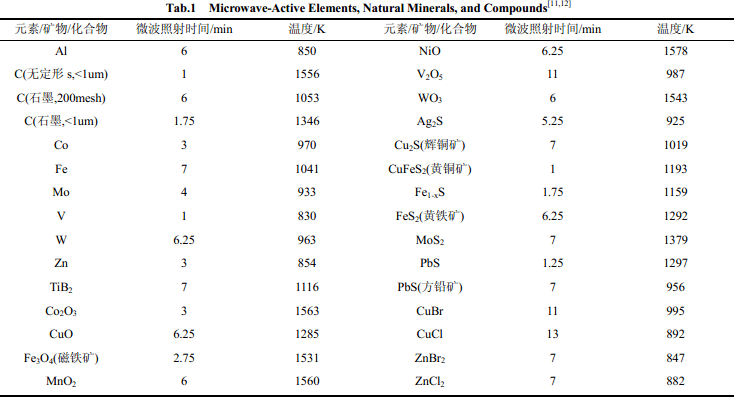
多数无机材料在常温下就可以与微波发生强烈的相互作用。表1列出了一些具有这样性质的矿物和无机化合物,并且给出了采用普通家用微波炉加热时这些材料的微波活性[11,12]。一些硫族化物,例如:HgS、MoS2、As2S3、ZnS等,它们也可以与微波相互作用,但是这些材料加热的速度比较慢,因此没有被列在表中。表中还包括一些过渡金属的氧化物、卤化物等,这些材料也可以利用微波进行快速加热。此外,各种类型的碳粉都可以与微波发生相互作用,使用功率为1kW、频率为2.45GHz的普通家用微波炉加热无定形碳的粉末,仅1min的时间便可以加热到1550K 。
利用微波加热电介质材料一般可称为介电加热[13]。材料中极性分子或可极化分子由于受到微波电场作用而发生极化,是这类材料可以利用微波加热的本质所在。当极性分子或可极性化分子在交变电场中发生极化时,电介质内部形成偶极矩,偶极矩顺着电场方向取向。如果电场的频率很低,介质分子的极化转向完全跟得上电场变化,那么基本上不消耗电场的能量。但当交变电场的频率提高时,由于介质分子的热运动及相邻分子之间的相互作用,转向受到摩擦阻力的影响,介质分子的极化转向运动相对于外电场就有滞后的现象,电场能量的消耗很大,以热的形式表现出来,使介质的温度升高。
当偶极矩的取向不具备迅速跟上交变电场的能力时,偶极矩在重新定位时就会产生相位差,从而引发与实际电场相协调的极化电流,材料内部便会发生阻抗加热。介质在微波场中的极化,表现为对电场电流密度的损耗,介质的复介电常数为 ε=ε’−iε″,式中,ε’为复介电常数的实部,其大小反映了介质束缚电荷的能力,ε’’为复介电常数的虚部,它反映了介质的损耗情况,故亦称介电损耗因子。实际电场的加热效应有一种更为方便的表示方法:tanδ=ε″/ε’,即用介电损耗因子与介电常数的正切表示物质在特定频率和温度下将电磁能转化为热能的能力。材料中的偶极矩可以自由转动,例如在液体中,电场能量的损耗是由偶极矩的转动频率来决定的。许多材料的偶极矩的特性与一个特定的驰豫时间τ密切相关,而介电常数由频率决定,如果偶极驰豫仅仅与单一的驰豫时间τ相关,而ω是微波场的角频率,那么介电量与频率之间的关系可以由德拜方程加以描述:

式中:εs 和ε∞分别是频率为0和无穷大时的介电常数;ε″随着频率变化而变化,当ωτ=1 或ω=1/τ时,ε″值将出现特定的峰值。对于 20℃的水,驰豫的峰频率大约是 18GHz 左右,而频率为 2.45GHz时,ε″将出现最大值,此时能量损耗快,水可以迅速升温,这便是普通微波炉的工作频率为2.45GHz的原因。
微波对材料的作用是非常复杂的,一方面反应物分子吸收微波能量,提高了分子的运动速度,使反应物分子的运动变得杂乱无章,从而导致反应过程中熵的增加;另一方面,微波对极性分子的作用,迫使其按照电磁场作用方向取向,又导致反应过程中熵的减小。因此微波对化学反应的作用机理是不能仅用微波的介电加热效应来描述的。微波对材料的作用除了具有上述的介电加热效应外,还存在一种与温度无关的特殊效应。由于微波的频率与分子的转动频率相近,微波被极性分子吸收时,可以通过在分子中储存微波能量与分子平动能量发生自由交换,即通过改变分子排列的焓或熵效应来降低反应活化能,这就是所谓的“非热效应”。微波作用下的化学反应,虽不足以使化学键断裂,但可以使化合物材料中某些化学键振动或转动,从而导致这些化学键的减弱,降低反应活化能,改变反应动力学。在微波作用下许多反应速度往往是常规反应的数十倍,甚至上千倍。然而,对于微波加速反应机理的研究,仍然是一个比较新的领域,有许多实验现象尚无法得到充分的论证和全面、细致与系统的解释,因此,还需要广大科学工作者去不断的探索。
微波加热不同于传统加热,传统加热是通过辐射、对流、传导三种方式由表及里进行的,而微波加热是材料在电磁场中由介电损耗而引起的体加热,其具有如下特点:
(1)体加热性。微波加热时,微波进入介质内部直接与介质作用,依靠介电损耗微波能而升温,具有体积加热性,因此可以在被加热物质的不同深度同时产生热,加热均匀,温度梯度小,有利于固化反应的进行。
(2)选择性加热。由于物质吸收微波能的能力取决于自身的介电特性,不同介质吸收微波的能力是不同的,对良导体,微波几乎全部被反射,因此良导体很难被微波加热;对电导率低、极化损耗又很小的微波绝缘体介质,微波基本上是全射透,一般也不易加热;而对那些电导率和极化损耗适中的介质,很容易吸收微波而被加热,因此微波能够对混合物中的各个组分进行选择性加热。在某些气固相反应中,同时存在气固界面反应和气相反应,气相反应有可能使选择性减小,利用微波选择性加热的特性就可使气相温度不致过高,从而提高反应的选择性。
(3)升温控制独特。微波加热是随微波的产生或消失而开始或终止的,微波加热无滞后效应,当关闭微波源后,再无微波能量传向物质,利用这一特性可进行对温度控制要求很高的反应。
(4)微波加热还具有热效应高、化学污染小或无污染、方法简便的特点。在单位时间和单位体积内,微波在介电加热过程中所耗散的功率 P 由总电流σ和电场强度E的平方所决定:
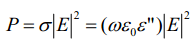
式中:P 为物质吸收微波的功率密度;ω为微波的角频率;ε0为真空中的介电常数;ε″为复介电常数中的介电损耗因子。上式还可利用ε’ 加以描述:

将德拜方程应用到上式,得到下式:
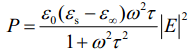
如果把与微波相互作用时的热量损失忽略不计,而且不考虑对周围环境的影响,加热速率可近似等于△T/t=ω| E|2/ρC,ρ表示材料的表观密度,C 表示材料的比热。
微波必须入射到材料的内部才能够使其得以加热,因此需要考虑微波在材料内部入射深度的问题。当微波垂直辐射于材料表面时,在材料内部入射强度沿着入射方向将迅速减小,就像微波能在迅速消散一样。这一现象可以通过渗透度D(渗透方向上的距离,指在渗透方向上能量减为最初值的一半时的深度)来描述。
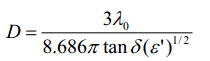
式中:λ0 为入射微波的波长。上式表明,一般吸收性介质的穿透深度大致和波长为同一数量级。以2.45GHz 的常用微波加热频率而言,通常吸收性介质的D值为几十厘米到几厘米,故除特大物体外,一般可以做到表里一致均匀加热。通过方程可以看出,当样品的量比较大时,使用低频微波是比较有利的。但是,根据每个个体吸收能量的不同,所消耗的能量又是不完全相同的。块体金属和合金材料,一般能够反射微波,它们的微波渗透度是非常浅的,可以利用趋肤深度η 加以描述[14]:
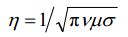
式中:ν为入射微波的频率(其入射微波的角频率ω=2πν),μ为真空磁导率,σ为材料的电导率。
材料的介电性能主要是由材料的化学成分和物理性质决定的,例如:材料的纯度、元素的化学态(是金属混合物还是氧化物)等能够引起高的介电损耗,导致强烈的微波耦合。同样地,表面缺陷,表面电荷和强的极化性能同样能够增强微波耦合的介电参数。维持永久极化的晶体结构也可以引起强烈的微波磁化,因此具有较高极化能力的材料可以用于微波基座。而具有压电效应的无机材料粉末能够引起吸收共振,这主要是由微波场中的颗粒振动引起的[14]。在离子材料中,极化效应和离子电流都能够使材料与微波发生强烈的耦合。
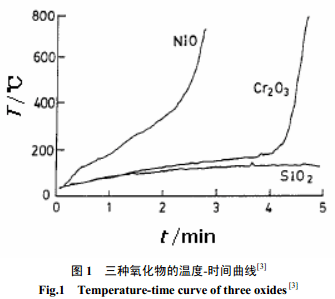
对于不同材料,其微波耦合性质是不同的。例如金属氧化物粉末与微波的作用可分为三种基本类型:第一类的物质一般都是变价化合物,如 NiO、MnO2、SnO2 等,它们有很强的吸收微波的能力,是一种高损耗物质,适宜作为微波诱导催化反应的催化剂;第二种类型的物质吸收微波的能力较弱,但它们经微波辐射一段时间后,表现出升温很快的特性,如Fe2O3、Cr2O3、V2O5等;第三类物质在微波场中升温很慢或基本上不升温,它们对微波是透明的,如Al2O3、TiO2等。同时,各种金属氧化物吸收微波的能力还随组分、结构的不同而有明显的差异。第一类物质在微波场中的升温速率约为 200/min℃,说明这类物质在微波场中有很高的活性,它们对微波极其敏感。第二类物质的微波升温曲线明显地出现一个拐点,也就是这类物质需要在场中辐射一段时间后,才出现温度的急剧上升,这种现象叫做热失控(或温度失控)。根据物质的不同,拐点出现的时间从 1.5~40min不等。第一类物质则表现出无拐点热失控。图1给出了三种氧化物的温度-时间变化曲线,说明了这一观点的正确性[3]。SiO2的介电常数和介电损耗的差别不大,尽管进行了长时间的微波辐射,仍然看不到明显的温度变化。但是,NiO和Cr2O3的温度在达到了一定的辐射时间后就开始不断上升。NiO 高的介电损耗使得温度直线升高,而 Cr2O3的介电损耗随着温度不断升高,某一时刻出现了温度的突然上升。图中升温速率出现突然增大的区域通常称为热量失控区。
接受微波照射时,大块金属与相应的金属粉末的变化是截然不同的。块体金属的趋肤深度十分小,并按δ/1的规律变化,因此,只有非常少量的微波能渗透进去。在大块金属样品和金属薄膜中,在微波腔内产生电场梯度,引起放电。而金属粉末中没有这样的放电现象发生,由于斡旋电流和局部等离子体区域的影响,很容易实现快速加热,其加热速率高达100K/s[15]。涡旋电流现象是由与微波相关的交互磁场引起的。受到磁场影响的微波耦合还有一些其它的现象,包括磁滞现象的减弱、磁场中的空间谐振及由孤对电子磁矩运动所引起的磁共振等[14]。
对于大多数材料而言,微波渗透度D值是非常高的,因此,只要材料的体积不是很大,微波能的损耗是贯穿始终的,这也是微波加热的重要特点,即,体加热,使得温度曲线沿着样品的几何边界出现迅速下降的趋势,这一点与传统加热方式完全不同。
2微波技术在无机固相材料制备中的应用
微波加热作为一种新的合成材料技术,由于具有其它方法尤其是传统合成技术不可比拟的优点,如反应速度快、合成时间短、反应条件温和、反应效率高、产品具有较高的纯度、窄的粒径分布和均一的形态等优点,因此适于推广到大规模的工业生产中去,在合成纳米材料、陶瓷材料等领域里显示了良好的发展态势和广阔的应用前景,已经受到各国广泛重视。微波技术应用于制备无机固相材料的方法总体上可分为湿法和干法。湿法,即微波辐射液相法,包括微波水热法、微波水解法、微波溶胶-凝胶法等;干法,即微波烧结法,包括固-固法和气-固法两种,由于湿法具有操作简单、污染少、粒子可控等优点,其研究更为广泛。
2.1微波辐射液相法-湿法
微波辐射液相法制备纳米微粒和陶瓷粉体是通过各种途径将均相溶液中的溶质和溶剂分离,溶质形成一定形状和大小的颗粒,从而得到所需的纳米微粒或陶瓷粉体。该液相法具有设备简单、原料容易获得、产物纯度高、均匀性好、化学组成控制准确等优点。微波辐射液相法包括微波简单照射法、微波水热法、微波水解法、微波溶胶-凝胶等,其中应用最广的是微波简单照射法、微波水热法。
2.1.1 微波简单照射法 微波简单照射法是以微波作为热源,在一定温度下通过简单液相反应来合成硫化物、氧化物以及磷灰石等纳米材料的一种新方法。利用该方法合成纳米材料具有反应时间短、产物颗粒小、分布均匀、纯度高等优点。因此,微波简单照射法是一种方便、快捷、有效的制备纳米无机材料的合成方法。
Xu等[16]利用微波简单照射法成功合成了尺寸可控的 YVO4 纳米颗粒,通过调节pH制备了不同尺寸的产物,其尺寸范围为 5~18nm,当 pH=7时产物颗粒尺寸最小,并且验证了随着产物颗粒尺寸的减小,红外峰出现蓝移,具有明显的量子尺寸效应。

Liu等[17]同样利用该方法通过调节pH成功地合成了具有棒状的、蝴蝶结状的、花状的羟基磷灰石纳米粉体,如图2。均匀纳米棒的直径为40nm,长为 400nm左右;蝴蝶结状的纳米颗粒是由宽为150nm,长为1~2μm 的剑状的纳米棒组成;而花状结构是由直径为150~200nm,长为1~2μm的叶状薄片构成。
2.1.2 微波水热法 该方法同样是以微波作为加热方式,结合传统的水热法来制备纳米粉体或陶瓷粉体的一种新方法。水热法是指在特制的密闭反应器(高压釜)中,采用水溶液作为反应体系,通过对反应体系加热、加压(或自生蒸气压),创造一个相对高温、高压的反应环境,使得通常难溶或不溶的物质溶解并且重结晶而形成无机固相材料的一种有效方法。然而,在传统的水热合成法中,往往是采用普通的传导加热方法,这种加热方式具有加热速率慢、反应时间长、热量分布不均匀、温度梯度大的等缺点,严重影响了合成粉体的性质、颗粒尺度等。采用微波加热可以使整个样品液体同时迅速升温,有效的缓解了普通传导加热带来不良影响。
印度国家化学研究所的Verma等[18]利用微波水热法在150℃、50Pa和25min的条件下成功制备了纳米相的 MgFe2O4,其平均尺寸在3nm 左右。经过测试,其具有良好的磁学性能。
2.1.3 微波溶胶-凝胶法 这种制备方法是在微波照射下,在一定的温度和条件下进行水解和缩聚反应,随着缩聚反应的进行以及溶剂的蒸发,具有流动性的溶胶逐渐变为略显弹性的固体凝胶,然后在比较低的温度下烧结成为所要合成的材料。该方法的优点是反应温度低,产物粒径小,合成工艺的可操作性强。
Komarneni等[19]对单相和两相莫来石凝胶进行微波辐照,合成了莫来石粉末。用微波对单相莫来石凝胶辐照10~15min,可得到纯的莫来石粉末;对两相凝胶进行微波辐照,合成的产品为α-Al2O3和莫来石的混合物。因此,用微波进行辐照时,与两相凝胶比较,通过单相凝胶合成莫来石更容易一些。微波所合成的纯莫来石粉末颗粒尺寸在 50nm~1μm之间波动。Kladig等[20]用微波辐照钡和钛的醋酸盐溶液得到干凝胶,然后继续用微波辐照加热,高温热解得到棕色产物后再用微波煅烧从而得到了无色的 BaTiO3粉末。
2.1.4 微波水解法 水解法是制备无机固相材料的常用方法之一,其关键是使沉淀相的核瞬间萌发,再让所有沉淀相的核尽可能同步生长成一定形状和尺寸的粒子。而微波水解法是将前驱体溶液置于微波场中,在微波作用下发生水解反应来制备无机固相材料的一种新方法。研究表明,微波水解法比常规水解法的反应速度快,缩短了材料的制备周期,基本上消除了温度梯度造成的影响,工艺简单易行。
汤利用微波水解法合成了分散形状为假立方体的氧化铁纳米粒子。表明了微波水解法可以在很短的时间内促使体系中生成大量的晶核,因而大大缩短了陈化时间。Bellon等[21]利用该方法在180℃的条件下,成功制备了尺寸为3~4nm的多晶氧化锆纳米颗粒;Li 等[22]同样利用该方法在不同反应条件下合成了不同形貌α-Fe2O3纳米粉体。
2.1.5 微波辅助化学浴沉积法(Microwave irradiation assisted chemical bath deposition, MA-CBD)这是一种以微波作为辅助加热方式,将经过表面活化处理的衬底浸在沉积液中,不外加电场或其它能量,在常压、低温(一般30~90℃)下通过控制反应物的络合和沉淀,从而在衬底上沉积薄膜的制备方法。
将微波辐射应用于化学浴过程,在衬底表面的成核可优先吸附溶液中的正负离子进行薄膜生长,抑制化学浴过程中其它副产物的形成。从而可调制薄膜生长过程中衬底-离子间的作用,就是说,可以促进在衬底表面的离子-离子异质生长。
Zhai 等[23]利用该方法通过微波照射在水浴中沉积10min,成功制备了闪锌矿结构CdS薄膜和纤锌矿结构ZnS薄膜,并通过测量和计算得出CdS和ZnS薄膜的带隙分别为2.51eV和3.91eV 。
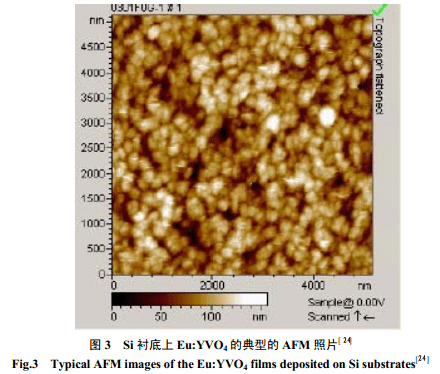
Xu等[24]利用微波辅助化学浴沉积法成功地制备了密实、附着力强、镜面的钒酸钇铕(Eu: YVO4)薄膜,其具有(200)择优取向,图3给出了在 Si衬底上沉积的 Eu:YVO4薄膜的典型的原子力显微(AFM)图片。由图可见,薄膜均匀密实,没有裂纹和针孔,由尺寸约为30~40nm的纳米颗粒紧密堆积而成。同时该薄膜还具有很好的 Eu3+5D0-7F2 发射性能。由于独特的微波介电加热更加快速有效,因此一些难以在传统CBD过程中发生的反应,有可能在微波辐射辅助的CBD条件下进行。从而为三元氧化物薄膜或其它一些无机材料的低温制备提供了一种切实有效的可行路线。
2.2 微波烧结法-干法
微波烧结法是自20世纪70年代发展起来的一种新的烧结技术。与传统烧结技术相比较,微波烧结法的速率更快,同时能够抑制晶粒长大、细化材料组织、改进材料性能。该方法是指用微波辐照代替传统热源,均匀混合的物料或预先压制成型的料坯通过自身对微波能量的吸收(或耗散)达到一定的高温,从而引发燃烧反应并最终完成合成过程。
2.2.1 微波固-固合成法 方法是以微波作为热源,在一定压力和温度下通过固相反应来合成纳米材料和陶瓷材料。该方法具有操作简单、反应时间短、无需后处理、产率高等优点。固体原料混合物以固态形式直接反应是制备无机固相材料最为广泛应用的方法。微波加热与传统加热技术相比较,它们属于两种截然不同的加热方式[25]:当用传统方式加热时,点火引燃总是从样品表面开始,燃烧波从表面向样品内部传播,最终完成烧结反应。而采用微波加热时,由于微波有较强的穿透力,能深入到样品的内部,首先使样品中心温度迅速升高达到着火点并引发燃烧反应,并沿径向从里向外传播,使整个样品几乎是均匀地被加热最终完成合成反应。因此能提高或改善合成产物的机械性能,并可根据对产物性质的要求,人为地控制燃烧波的传播。
微波固-固合成法与传统固相法相比,最大的特点是反应速度大幅度提高,传统固相法需几天完成的反应,微波固相法仅需十几分钟或几个小时即可完成反应,且产率较高。Cheng等[26]把TiO2、BaCO3、Pb3O4 混合后用 60MPa 的压力把混合物压成圆片,放在微波场中,在750℃温度下辐照 10min,合成了(PbxBa1−x)TiO3。而用传统合成法,在 850℃的温度下至少需要2h,并且微波合成过程中减少了氧化铅的挥发损失。
Chen等[27]利用微波固-固合成法成功制备了(1−x)(0.94PbZn1/3Nb2/3O3+0.06BaTiO3)+ x PbZryTi1−yO3(PZN-PZ-PT) 陶瓷。与传统烧结方法合成的产物(1150℃,2h)相比,微波固-固合成法制备的产物(1150℃,10min) 拥有高的介电常数,产物的晶界处元素分离状况明显减少。表明该方法不但能增加产物的密度,而且能够有效地减少PbO/ZnO的分离和无定形颗粒层的形成,极大地改进了PZN-PZ-PT 的电学性能。Thakur 等[28]以BaCO3、SrCO3 和TiO2 为原料采用该方法成功制备了 Bao0.5Sr0.5TiO3 陶瓷材料,与传统方法相比,产品具有密度高、微结构和导电性好、粒度细、线性热膨胀高等特点。
2.2.1 微波气-固合成法 该方法是首先将原料配制好,然后在特定的气体氛围中利用微波能加热原料,从而使原料与气体发生化学反应来快速地合成陶瓷材料。与常规加热合成相比微波合成具有很大的优越性,不但可以大大地降低合成温度、极大地缩短合成时间,而且能够得到超细、高纯的产品。
Kiggans 等[29]在氮气氛中用微波辐照高纯硅,在低温下氮化得到了氮化硅,并与传统方法进行了比较。结果表明,微波辐照时,99.95%纯硅的氮化温度始于1200℃,而传统加热时的氮化温度始于1250℃,同时微波辐照下的氮化率高于传统加热下的氮化率。
Liu以TiO2和碳粉为原料,在氮气氛围中,采用频率为2.45GHz、功率为5kW的微波设备合成了高纯的、平均粒度为 1~2μm的TiN粉末。他们指出,常规碳热还原法合成的温度为1300~1800℃,时间为15h,而用微波合成法在1200 ℃下碳热还原TiO2,仅用1h就可合成出高纯的TiN 粉末。合成温度的降低及合成时间的缩短是微波热效应和非热效应共同作用的结果。一方面,由于微波加热均匀迅速,缩短了升温周期;另一方面,非热效应使原子、分子、离子等微观粒子得到活化,使晶格和晶界扩散等加快,扩散活化能大大降低,反应物间的物质迁移加速,反应活化能也因此降低,从而使 TiN 合成温度降低了 100~200℃,合成周期缩短为常规法的 1/30~1/15。
3 结语
微波作为一种新型高效的加热方式,在材料化学领域中所显示出的清洁、高效、低能耗、收率高及选择性好等优点,使其在材料制备及化学中得到广泛应用,但微波技术毕竟是一门新兴的学科,其发展还处于初级阶段,有许多问题尚待进一步研究,比如:微波如何改变反应的活化能,微波功率、微波宽度、脉冲频率如何影响反应等;另外,目前微波实验所用设备大多是改性的家用微波炉,这样的实验设备有许多局限性,因此,研制、开发、生产出适合于微波实验的专用设备,也是急需解决的问题之一。随着研究的不断深入,相信以上问题将逐一得到解决,微波技术在材料合成及化学领域将获得更广泛应用和更迅速发展。
参考文献
[1] L M Sheppard. Ceram. Bull., 1988, 67: 1656~1661.
[2] D Michael, D R Baghurst, D M P Mingos et al. Chem. Soc. Rev., 1991, 20: 1~47.
[3] D M P Mingos, D R Br Baghurst. Ceram. Trans. J., 1992, 91: 124~127.
[4] D M P Mingos. Chem. Ind., 1994: 596~599.
[5] K J Rao, P D Ramesh. Bull. Mater. Sci., 1995, 18: 447~465.
[6] D E Clark, W H Sutton. Annu. Rev. Mater. Sci., 1996, 26: 299~331.
[7] K G Ayappa. Rev. Chem. Eng., 1997, 13: 1~14.
[8] V M Kenkre, L Skala, M W Weiser et al. Mater. Sci., 1991, 26: 2483~2489.
[9] K Y Lee, E D Case, J Asmussen et al. Mater. Res. Innovat., 1997, 1: 101~108.
[10] K J Rao, B Vaidhyanathan, M Ganguli et al. Chem. Mater., 1999, 11: 882~895.
[11] J W Walkiewicz, G Kazonich, S L Mcgill. Miner. Metall. Process., 1988, 5: 39~42.
[12] R G Ford. Mater. Process. Rep., 1988, 3: 1~19.
[13] C Gabriel, S Gabriel, E H Grant et al. Chem. Soc. Rev., 1998, 27: 213.
[14] R E Newnham, S J Jang, M Xu et al. Ceram. Trans., 1991, 21: 51~56.
[15] A G Whittaker, D M P Mingos. J. Chem. Soc., 1992: 2751~2766.
[16] H Y Xu, H Wang, H Yan et al. Solid State Commu., 2004, 130: 465~468.
[17] J B Liu, H Wang, H Yan et al. Nanotechnology, 2005,16: 82~87.
[18] S Verma, P A Joy, Y B Khollam et al. Mater. Lett., 2004,58: 1092~1095.
[19] S Komarneni, T C Simonton, R Roy et al. Mat. Res. Symp. proc. [J], 1988,124: 235~237.
[20] W E Kladig, A J Luffman, R L Beatty et al. Ceram. Internat. [J], 1990,16: 99~106.
[21] K Bellon, D Chaumont. J.Mater.Res., 2001,16:2619~2622.
[22] Q li, Y Wei. Mater. Res. Bull., 1998,33: 779~782.
[23] R Zhai, H Wang, H Yan et al. Mater. Lett., 2005,59: 1497~1501.
[24] H Y Xu, H Wang, H Yan et al. Nanotechnology, 2005,16: 65~69.
[25] J S Li, J F Zhang. Petrochemical Industry Tech., 2002,9(3): 178~183.
[26] J P Cheng, A Dinesh, R Rustum et al. Mat. Ros. Soc. Symp. Proc. [J], 1994, 347: 513~518.
[27] C L Li, C C Chou. J. Euro. Ceram. Soc., 2006, 26: 1237~1244.
[28] O P Thakur, C Prakash, D K Agrawal. Mater. Sci. Eng. B, 2002, 96: 221~225.
[29] J O Kiggans, M Subirats, M F Iskander et al. Ceram. Transact. [R], 1991,21: 403~410.
注:本文为提供者整理翻译的,由于知识所限,错误在所难免,敬请原谅。如有问题可以查找原文。



 沪公网安备 31010602001115号
沪公网安备 31010602001115号